Кислородът е химичен елемент. Той има символ О и атомен номер 8. Той е третият най-разпространен елемент във Вселената след водорода и хелия.
Кислородът е повече от една пета от обема на земната атмосфера. Във въздуха два кислородни атома обикновено се съединяват, за да образуват диоксиген (O
2) - безцветен газ. Този газ често се нарича просто кислород. Той няма вкус или мирис. Когато е в течно или твърдо състояние, той е бледосин.
Кислородът е част от халкогенната група в периодичната таблица. Той е много реактивен неметал. Той образува оксиди и други съединения с много елементи. Кислородът в тези оксиди и в други съединения (предимно силикатни минерали и калциев карбонат във варовика) съставлява почти половината от земната кора по маса.
Повечето живи същества използват кислород при дишането. Много молекули в живите организми съдържат кислород, като например протеини, нуклеинови киселини, въглехидрати и мазнини. Кислородът е част от водата, от която се нуждае всичко живо, за да живее. Водораслите, цианобактериите и растенията произвеждат газообразния кислород на Земята чрез фотосинтеза. Те използват светлината на Слънцето, за да получат водород от водата, при което се отделя кислород.
В горната част на земната атмосфера се намира озонът (O
3) в озоновия слой. Той поглъща ултравиолетовата радиация, което означава, че до земната повърхност достига по-малко радиация.
Кислородният газ се използва за производство на стомана, пластмаси и текстил. Той има и медицинско приложение и се използва за дишане при липса на добър въздух (например от водолази и пожарникари), както и за заваряване. Течният кислород и богатите на кислород съединения могат да се използват като ракетно гориво.
Физични и химични свойства
Атомни и молекулни характеристики: Атомната маса на кислорода е приблизително 15.999 u. Електронната конфигурация на атома е 1s2 2s2 2p4. Най-разпространената форма в природата е диатомната молекула O
2, която е парамагнитна поради наличието на два неспарени електрона в анти-обвързващите π* орбитали.
Фазови преходи и плътности: Точката на топене на кислорода е около −218.79 °C (54.36 K), а точката на кипене ≈ −182.96 °C (90.19 K). Плътността на газа при стандартни условия е приблизително 1.429 g·L−1, докато течният кислород е бледосин и има висока плътност спрямо газообразната форма.
Химична активност и състояния на окисление: Кислородът е силно реактивен неметал и най-често проявява степен на окисление −2 (въглеродни и метални оксиди). Съществуват и форми като пероксиди (степен −1) и супероксиди (степен −1/2). Той образува оксиди с почти всички елементи и участва в горещи окислителни реакции.
Алотропни форми и изотопи
Алотропи: Основните алотропи са диоксиген (O
2) и озон (O
3). Озонът е силен окислител с характерна миризма и син цвят в концентрирани количества; в стратосферата той играе защитна роля срещу ултравиолетовата радиация, но на земната повърхност е вреден замърсител.
Изотопи: Природният кислород се състои предимно от стабилния изотоп 16O (~99.76%), с малки количества 17O и 18O. радиоактивни изотопи също са известни, но са редки и имат кратки времена на полуразпад.
Разпространение в природата
Кислородът е един от най-разпространените елементи на Земята — съставлява почти половината от масата на земната кора и е основен компонент на вода (H2O), минерали (особено силикатите) и органични съединения. В атмосферата той присъства основно като O
2 (~20.95% по обем).
Биологична роля
Кислородът е незаменим за аеробните организми: той служи като краен акцептор на електрони в клетъчното дишане, което освобождава енергия за метаболитни процеси. Молекули като протеини, нуклеинови киселини, въглехидрати и мазнини съдържат кислород и участват в структурни и енергийни функции. Фотосинтезиращите организми (растения, водорасли, цианобактерии) генерират кислород като страничен продукт на преобразуването на слънчевата енергия във въглехидрати.
Производство и промишлена употреба
- Основен промишлен метод за получаване на кислород е фракционната дестилация на течен въздух, при която се отделят азот, кислород и благородни газове.
- Електролизата на вода произвежда високопurity кислород и е важна в лаборатории и за специфични индустриални приложения.
- Приложения: производство на стомана, химическа индустрия за окислителни процеси, текстил, пластмаси, медицинско използване като терапевтичен кислород, спасителни дейности (водолази, пожарникари), заваряване и използване на течен кислород като ракетно гориво (окислител).
Безопасност и рискове
Поддържане на изгаряне: Кислородът сам по себе си не е запалимо вещество, но значително усилва изгарянето: материали, които не горят добре на въздух, могат да се възпламенят лесно в обогатена с кислород среда.
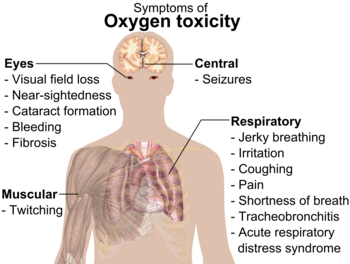
Кислородна токсичност: При по-високи от атмосферните парциални налягания на кислорода (например при гмуркане или при продължителна употреба на 100% кислород) може да настъпи токсичен ефект върху централната нервна система и белите дробове.
Криогенното съхранение: Течният кислород е екстремно студен и изисква специални съдове; контактът с кожа може да предизвика измръзване. Освен това може да предизвика неочаквани реакции при контакт с органични материали и мазнини.
Кратка историческа бележка
Кислородът е открит независимо през 1770-те години от учените Карл Вилхелм Шееле и Джоузеф Пристли; Антоан Лавоазие обяснява ролята му в горенето и в процесите на окисление и дава името "кислород" (от гръцки: "производител на киселини") — термин, който по-късно се оказва неточен за много вещества, но остава в употреба.
Интересни факти
- Елементът е жизненоважен за повечето висши форми на живот на Земята, но някои организми са анаеробни и живеят без кислород.
- Изотопният състав на кислорода (особено 18O/16O) се използва в климата и палеоклимата за реконструкция на минали температури и климатични условия.
- Кислородът на Земята е следствие от милиарди години фотосинтетична активност и промяната в неговото количество през геоложкото време е свързана с еволюцията на живота и атмосферата.