Химичната реакция се случва, когато едно или повече химични вещества се превръщат в едно или повече други химични вещества. Примери:
- желязото и кислородът се съединяват, за да образуват ръжда
- оцет и сода за хляб се комбинират, за да се получи натриев ацетат, въглероден диоксид и вода
- горящи или експлодиращи неща
- много реакции, които протичат в живите организми.
- електрохимични реакции при разреждане или зареждане на батерии.
Някои реакции са бързи, а други - бавни. Някои протичат с различна скорост в зависимост от температурата или други фактори. Например дървото не реагира с въздуха, когато е студено, но ако се нагрее достатъчно, ще започне да гори. При някои реакции се отделя енергия. Това са екзотермични реакции. При други реакции се приема енергия. Това са ендотермичниреакции.
Ядрените реакции не са химични реакции. При химичните реакции участват само електроните на атомите, а при ядрените реакции - протоните и неутроните в атомните ядра.
Какво още трябва да знаете за химичните реакции
Основни характеристики
- При химична реакция се променя начинът, по който атомите са свързани помежду си; образуват се нови вещества със стъпни свойства.
- В процеса на реакция важат закона за запазване на масата и закона за запазване на елементарните видове: общият брой и вид на атомите преди и след реакцията е един и същ.
- Химичната реакция често се представя чрез химично уравнение: aA + bB → cC + dD, където коефициентите се балансират, за да се запази масата.
Видове химични реакции (по обща класификация)
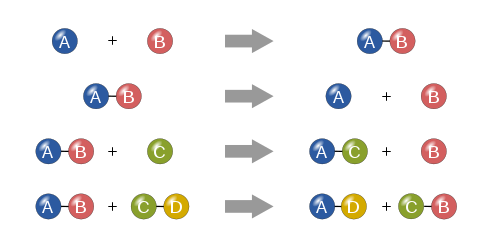
- Синтез (образуване): два или повече реагента образуват един продукт. Пример: A + B → AB (на практика: 2H2 + O2 → 2H2O).
- Разлагане (деокомпозиция): едно вещество се разпада на две или повече. Пример: 2H2O2 → 2H2O + O2 (при катализатор).
- Заместителна (едновалентно заместване): един елемент замества друг в съединение. Пример: Zn + 2HCl → ZnCl2 + H2.
- Обменна (двойно заместване): йонен обмен между два съединения. Пример: AgNO3 + NaCl → AgCl↓ + NaNO3.
- Горене (комбустион): бърза реакция с кислород, често отделяща топлина и светлина. Пример: CH4 + 2O2 → CO2 + 2H2O.
- Окислително-редукционни (редокс): прехвърляне на електрони; изменения в степен на окисление на елементите. Пример: 2Fe + O2 → 2FeO (частен случай).
- Киселинно-основни (нейтрализация): киселина + основа → сол + вода. Пример: HCl + NaOH → NaCl + H2O.
- Полимеризация: образуване на дълги вериги (полимери) от мономери. Пример: nCH2=CH2 → −(CH2−CH2)n− (полимеризация на етилен).
- Фотохимични реакции: реакции, инициирани от светлина (напр. фотосинтеза частично прифотохимична).
- Електрохимични реакции: протичат чрез електронен поток при електроди (в батерии, електролиза).
- Биохимични/ензимни реакции: каталитично протичащи реакции в живите организми, често със силна специфичност и при умерени условия на температура и рН.
Фактори, които влияят на скоростта на реакциите
- Температура: по-високата температура обикновено увеличава скоростта, защото повече частици имат енергия над активиращата бариера.
- Концентрация: по-голяма концентрация на реагентите води до повече сблъсъци между молекулите и по-бърза реакция.
- Повърхностна площ: при твърди реагенти по-голямата повърхност ускорява реакцията (например прахообразни реагенти реагират по-бързо от груби парчета).
- Катализатори и инхибитори: катализаторите намаляват енергията на активация и ускоряват реакцията, без да се консумират; инхибиторите я забавят.
- Налягане: важи особено за газови реакции — увеличение на налягането (намаляване на обема) води до по-висока честота на сблъсъци.
- Природа на реагиращите вещества: химическата структура и наличието на връзки, които лесно се разкъсват, определят склонността за реакция.
Енергия и термодинамика
- Екзотермични реакции: отделят енергия (топлина), например горенето. Показател: общата енергия на продуктите е по-ниска от тази на реагентите.
- Ендотермични реакции: поглъщат енергия (топлина), например термично разлагане.
- Активираща енергия: минималната енергия, необходима за началото на реакцията; катализаторите намаляват тази бариера.
- Химичен баланс и равновесие: при обратими реакции установява се динамично равновесие, описвано от константата на равновесие (K). Принцип на Ле Шателие: промени в условията (температура, налягане, концентрация) преместват равновесието.
Как да разпознаем, че протича химична реакция
- Поява на газ (бълбукане), когато няма механична причина.
- Образуване на твърд утайка (преципитат).
- Промяна на цвета.
- Отделяне или поемане на топлина (затопляне или охлаждане на средата).
- Излъчване на светлина или звук (при експлозии или горене).
Значение и приложения
- Индустрия: производство на торове, горива, пластмаси, фармацевтични вещества и др.
- Енергетика: реакции при горене, в горивни клетки и батерии осигуряват енергия.
- Биология и медицина: метаболитни реакции поддържат живота; синтез на лекарства зависи от контролирани химични реакции.
- Околна среда: реакции определят качеството на въздуха, водата и почвите (напр. корозия, разграждане на замърсители).
- Наука и технологии: материалознание (нови сплави, наноматериали), катализатори, синтез на специални съединения.
Разбирането на химичните реакции и контролът върху тях са ключови за безопасна работа, ефективни производствени процеси и развитие на нови технологии. За важни понятия като запазване на масата, балансиране на уравнения и видове реакции е полезно да се упражнявате с конкретни уравнения и експерименти под наблюдение в учебна или лабораторна среда.