Въглеродът е много важен химичен елемент с химичен символ С. Той е необходим на всички познати видове живот на Земята. Въглеродът има атомна маса 12 и атомен номер 6. Той е неметал, което означава, че не е метал.
Когато желязото се легира с въглерод, се получава твърда стомана. Въглеродът под формата на въглища е важно гориво.
Физични и химични свойства
Въглеродът е химически много гъвкав елемент. Има четири валентни електрона, което му позволява да образува стабилни единични, двойни и тройни ковалентни връзки с други въглеродни атоми и с много други елементи. Тази способност да свързва дълги вериги от атоми (кацетиране) е основата на органичната химия и на богатото разнообразие от въглеродни съединения.
- Атомни данни: атомен номер 6; относителна атомна маса ≈ 12.011 (стандартна стойност за естествено срещащ се въглерод).
- Оксидни състояния: най-често +4 и +2 в неорганични съединения; в органичните молекули обикновено се разглежда като образуващ ковалентни връзки.
- Химична активност: сам по себе си чистият въглерод е относително инертен при стайна температура, но реагира при високи температури (изгаряне, карбонизационни процеси).
Алотропни форми
Въглеродът съществува в няколко алотропни форми с много различни свойства:
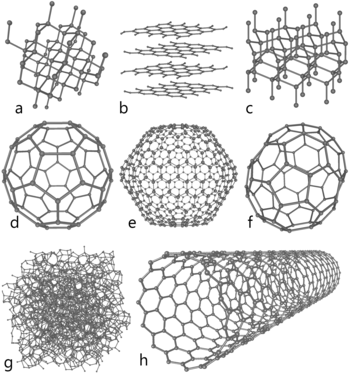
- Диамант – кристална решетка, където всеки въглероден атом е тетраедрично свързан с четири други; изключително твърд, прозрачен, отличен топлинен проводник.
- Графит – слоеста структура; силни връзки в рамките на слоевете, а слабите връзки между слоевете позволяват плъзгане (поява на смазващи свойства и използване в моливи и електроди).
- Графен – единичен слой въглеродни атоми в шестоъгълна мрежа; уникални електронни и механични свойства, важен за нанотехнологиите.
- Фулерените и въглеродните нанотуби – сферични и тръбни структури с обещаващи приложения в електроника, материали и медицина.
- Аморфен въглерод – включва въглен, сажди и активен въглен; различава се по порьозност и повърхностни свойства.
Роля в живота и биологията
Въглеродът е фундаментален градивен елемент за всички биомолекули: въглехидрати, липиди, протеини, нуклеинови киселини (ДНК и РНК) и множество други метаболити. Органичната химия е науката за съединенията на въглерода. Основни процеси, свързани с въглерода в природата:
- Фотосинтеза: растенията и някои микроорганизми преобразуват CO2 в органични молекули, като използват слънчева енергия.
- Дишане и разлагане: при клетъчното дишане и разлагането на органично вещество се отделя въглерод под формата на CO2 или метан (CH4).
- Въглероден цикъл: обменът на въглерод между атмосферата, хидросферата, литосферата и биосферата регулира климата и плодородието.
Промишлени приложения
Въглеродът и неговите съединения имат широк спектър от приложения в индустрията:
- Металообработка: добавянето на въглерод към желязото (легиране) променя свойствата и води до образуване на стомана с различна твърдост и якост.
- Горива: Въглища, нефт и природен газ са основни източници на енергия; остатъчни продукти от тях, като кокс, се използват в металургията.
- Пластмаси и синтетични материали: органичните полимери са изградени от въглеродни мономери (полиестер, полиетилен, полипропилен и др.).
- Специални материали: въглеродни влакна (carbon fiber) за леки и здрави конструкции; активен въглен за пречистване и филтрация; диаманти за режещи инструменти.
- Електроника и нанотехнологии: графен, въглеродни нанотуби и фулерени се проучват за приложения в електроника, сензори и медицински устройства.
- Енергетика и акумулатори: въглеродни електроди, катализатори и материали за акумулатори и горивни клетки.
Изотопи и приложения
- C‑12 – най-разпространеният стабилен изотоп; стандарт за относителна атомна маса.
- C‑13 – стабилен, използва се в ЯМР спектроскопия и като маркер в биологични и екологични изследвания.
- C‑14 – радиоактивен, широко използван за датировка (въглеродно датиране) на археологични и геоложки образци.
Въглерод и околна среда
Съединенията на въглерода, особено въглеродният диоксид (CO2) и метанът (CH4), играят ключова роля в парниковия ефект и глобалното затопляне. Изгарянето на изкопаеми горива освобождава големи количества CO2 в атмосферата, което води до промени в климата. Намаляването на емисиите, улавянето и съхранението на въглерод (CCS) и преходът към възобновяеми източници са сред основните мерки за ограничаване на въздействието.
Как се добива и използва
- Елементарният въглерод се добива чрез коксуване на въглища, преработка на нефт и други карбонизиращи процеси.
- Органични съединения богати на въглерод се произвеждат чрез синтез и рефинерия на петрохимични продукти.
- Напредъкът в синтеза на нови въглеродни материали (графен, нанотрубки, композити) разширява приложенията в бъдещите технологии.
Ключови факти — обобщение
- Въглеродът е основният елемент на живота и на голяма част от материалите, с които работим.
- Алотропните му форми определят широкия диапазон от физични и химични свойства.
- Икономическите и екологичните последици от употребата на въглеродни горива правят управлението на въглеродните емисии важен глобален приоритет.
Този преглед дава обща картина на свойствата, биологичната значимост и промишленото значение на въглерода. За по-задълбочена информация в определена област (напр. наноматериали, енергетика или органична химия) може да се разгледат специализирани източници или да зададете конкретен въпрос.