Ковалентна връзка: определение, образуване, полярност и примери
Ковалентна връзка — определение, образуване, полярност и примери за вода и други молекули, ясно обяснение на електрони и валентни обвивки за ученици и любопитни читатели
Ковалентните връзки са вид химични връзки, които се установяват главно между два неметални атома. При тях атомите споделят един или повече валентни електрони, за да постигнат по-стабилна електронна конфигурация (често следвайки правилото за октет). Класически пример е водата, където водородът (H) и кислородът (O) са свързани чрез ковалентни връзки в молекулата (H2O).
Как се образува ковалентна връзка
Атомите имат електрони, разпределени в електронни обвивки; валентните електрони са тези в най-външния слой и участват активно в химичните връзки. Броят на електроните в атома се определя от броя на протоните в него и от общата електронна конфигурация. Първият електронен слой по правило побира до два електрона, следващите — обикновено до осем (правилото за октет), макар че има изключения.
Ковалентната връзка се формира, когато два атома споделят една или повече двойки валентни електрони. При приближаване на два атома се появява обща електронна орбитала, която обхваща и двете ядра; електроните в тази орбитала имат по-ниска енергия, отколкото в отделните атомни орбитали, което прави системата по-стабилна. При образуването на връзката се освобождава енергия; за разкъсването ѝ е необходимо приблизително същото количество енергия.
Типове ковалентни връзки
- Единична връзка — споделяне на една двойка електрони (например H–H, в молекулата на водорода).
- Двойна връзка — споделяне на две двойки електрони (например O=O в кислорода).
- Тройна връзка — споделяне на три двойки електрони (например N≡N в азота).
- Координатна (дативна) връзка — и двете свързващи електрони предоставя един атом (например в някои комплексни йони и молекули).
- Резонанс — при някои молекули истинската структура е хибрид на няколко възможни разпределения на електроните (например нитратния анион).
Полярност на ковалентните връзки
Полярността зависи от разликата в електроотрицателността между свързаните атоми. При равномерно споделяне (малка или нулева разлика) връзката е неполярна ковалентна. Ако един от атомите привлича електроните по-силно, споделената електронна двойка се измества към него и връзката става полярна ковалентна, с частични заряди (δ+ и δ−) в краищата на връзката.
Като ориентир (стойностите са приблизителни):
- Разлика на електроотрицателност ~0–0.4: неполярна ковалентна
- ~0.4–1.7: полярна ковалентна
- >~1.7: предимно йонна (въпреки че реалните граници са условни)
Пример: в водата, кислородът е по-електроотрицателен от водорода и привлича споделените електрони повече. В резултат кислородният атом има частичен отрицателен заряд (δ−), а всеки водороден атом — частичен положителен заряд (δ+). Това прави молекулата полярна: зарядът ѝ не е равномерно разпределен, а има електрически диполен момент.
Свойства, свързани с ковалентните връзки
- Дължина и енергия на връзката: двойните и тройните връзки са по-къси и по-стабилни (по-енергийно изискващи за разкъсване) от единичните.
- Силна зависимост от ориентацията: ковалентните връзки имат определена геометрия (ъгли и пространствено разположение), която определя формата на молекулата (например тетраедрична форма в метана).
- Химична реактивност: местата с полярни връзки или НЕзапълнени орбитали са често реактивни центрове.
- Междумолекулни взаимодействия: полярните ковалентни молекули (като водата,) могат да образуват водородни връзки, което обяснява много от уникалните свойства на водата (висока точка на кипене, повърхностно напрежение и т.н.).
Чести примери
- H2 — единична неполярна ковалентна връзка между два водородни атома.
- O2 — двойна ковалентна връзка между два кислородни атома.
- N2 — тройна ковалентна връзка между два азотни атома (много стабилна молекула).
- HCl — полярна ковалентна връзка; H е δ+, Cl е δ−.
- CH4 — четири еднинини ковалентни връзки между въглерод и водород; молекулата е неполярна заради симетрията.
- CO — ковалентна връзка с частично йонен характер и резонансни структури; въглеродът и кислородът участват и в донорно-приемни взаимодействия.
Изключения и допълнителни бележки
Правилото за октет не е абсолютно: някои елементи (напр. Be, B) могат да образуват стабилни съединения с по-малко от 8 електрона, докато елементи от трети период и над него (напр. P, S) могат да разширят своя октет. Също така границата между ковалентна и йонна връзка е постоянен континуум, а не рязка разделителна линия.
Ковалентните връзки са фундаментални за строежа на органичната и неорганичната химия и определят множество физични и химични свойства на веществата. Разбирането на техните видове, полярност и геометрия помага да се прогнозира реактивността и поведението на молекулите в различни условия.
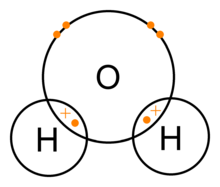
Ковалентни връзки на водата (H2O)
Видове ковалентни връзки
Атомните орбитали (с изключение на s-орбиталите) създават различни видове ковалентни връзки:
- Сигма (σ) връзките са най-здравите ковалентни връзки. При тях орбиталите на два различни атома се припокриват. Обикновено единичната връзка е σ връзка.
- Pi (π) връзките са по-слаби и се дължат на странично припокриване между p (или d) орбитали.
- Двойната връзка между два дадени атома има една σ и една π връзка, и
- тройната връзка има една σ и две π връзки.
Ковалентните връзки са по-слаби от йонните и имат по-ниска температура на топене. Освен това като цяло те са лоши проводници на електричество и топлина.
Дължина на връзката
В химията дължината на връзката е мярка за размера на ковалентната връзка. Тъй като молекулите са много малки, те се измерват в пикометри, или около една милионна част от милиардната част на метъра.
Химията на молекулите се обяснява най-вече с техните връзки, а връзките се дължат на структурата на електроните.
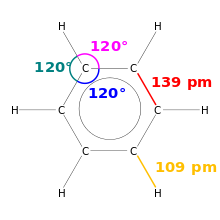
Рисуване на бензен. Показани са дължините на връзките и ъглите на връзките.
Свързани страници
- Валентност
Въпроси и отговори
В: Какво представлява ковалентната връзка?
О: Ковалентната връзка е химична връзка между два неметални атома, при която атомите споделят валентни електрони. Това създава електронна орбитала, която е свързана с двете атомни ядра и има по-ниско енергийно ниво от първоначалната електронна орбитала. В резултат на това атомът, който е предоставил електрона, има малък нетен положителен заряд, а другият атом - малък нетен отрицателен заряд, които се държат заедно чрез електромагнитна сила на привличане между положителните и отрицателните заряди.
Въпрос: Колко електрона обикновено има един атом във външната си обвивка?
О: Външната обвивка на атома обикновено съдържа до осем електрона или два в случая на водорода или хелия.
В: Какво определя броя на електроните в един атом?
О: Броят на електроните в атома се определя от броя на протоните в него.
В: Как се образуват ковалентните връзки?
О: Ковалентните връзки се образуват, когато атомите се доближат един до друг и един слабо задържан електрон от единия атом прескочи в нова орбитала, която е свързана с двете атомни ядра с по-ниско енергийно ниво от предишното. В резултат на това единият атом има малък нетен положителен заряд, а другият - малък нетен отрицателен заряд, което създава електромагнитна сила на привличане между тях.
Въпрос: Какъв тип молекула е водата?
О: Молекулите на водата се състоят от един кислороден атом и два водородни атома, свързани помежду си с ковалентни връзки, което я прави полярна молекула, тъй като зарядът ѝ не е равномерно разпределен.
В: Къде обикалят електроните около атомните ядра?
О: Електроните обикалят около атомните ядра като размити орбитални пътища.
обискирам