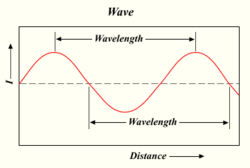
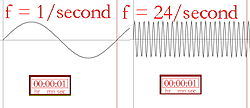
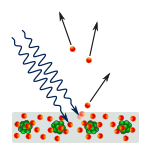
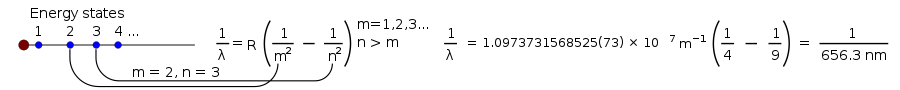Формулите и идеите на квантовата механика са създадени, за да обяснят светлината, която идва от нажежения водород. Квантовата теория на атома трябваше също така да обясни защо електронът остава в своята орбита, което другите идеи не бяха в състояние да обяснят. От по-старите идеи следваше, че електронът би трябвало да попадне в центъра на атома, тъй като в началото той се задържа в орбита благодарение на собствената си енергия, но бързо губи енергията си, докато се върти в орбитата си. (Това е така, защото беше известно, че електроните и другите заредени частици излъчват светлина и губят енергия, когато променят скоростта си или се въртят.)
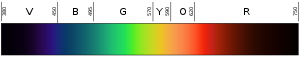
Водородните лампи работят като неонови лампи, но неоновите лампи имат своя собствена уникална група от цветове (и честоти) на светлината. Учените научават, че могат да идентифицират всички елементи по цветовете на светлината, която произвеждат. Само че не са могли да разберат как се определят честотите.
След това швейцарски математик на име Йохан Балмер съставя уравнение, което показва каква ще бъде λ (ламбда - дължина на вълната):
λ = B ( n 2 n 2 - 4 ) n = 3 , 4 , 5 , 6 {\displaystyle \lambda =B\left({\frac {n^{2}}{n^{2}-4}}\right)\qquad \qquad n=3,4,5,6} 
където B е число, което Балмър определя като равно на 364,56 nm.
Това уравнение работи само за видимата светлина от водородна лампа. По-късно обаче уравнението е направено по-общо:
1 λ = R ( 1 m 2 - 1 n 2 ) , {\displaystyle {\frac {1}{\lambda }}=R\left({\frac {1}{m^{2}}}-{\frac {1}{n^{2}}}\right),} 
където R е константата на Ридберг, равна на 0,0110 nm−1 , а n трябва да е по-голямо от m.
Ако се въведат различни числа за m и n, е лесно да се предскажат честотите за много видове светлина (ултравиолетова, видима и инфрачервена). За да видите как става това, отидете на сайта на Хиперфизика и слезте до средата на страницата. (Използвайте H = 1 за водород.)
През 1908 г. Уолтър Риц създава принципа на комбинацията на Риц, който показва как определени интервали между честотите се повтарят. Това се оказва важно за Вернер Хайзенберг няколко години по-късно.
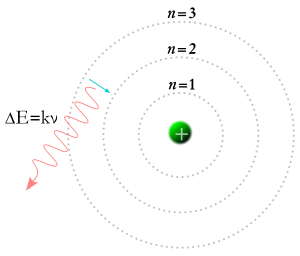
През 1905 г. Алберт Айнщайн използва идеята на Планк, за да покаже, че светлинният лъч се състои от поток частици, наречени фотони. Енергията на всеки фотон зависи от неговата честота. Идеята на Айнщайн поставя началото на идеята в квантовата механика, че всички субатомни частици като електрони, протони, неутрони и други са едновременно и вълни, и частици. (Вижте снимката на атома с електрона като вълна в атома.) Това води до теорията за субатомните частици и електромагнитните вълни, наречена дуализъм вълна-частица. При него частиците и вълните не са нито едното, нито другото, а имат определени свойства и на двете.
През 1913 г. Нилс Бор стига до идеята, че електроните могат да заемат само определени орбити около ядрото на атома. Според теорията на Бор числата, наречени m и n в горното уравнение, могат да представляват орбити. Теорията на Бор гласи, че електроните могат да започнат на някаква орбита m и да завършат на някаква орбита n, или електронът може да започне на някаква орбита n и да завърши на някаква орбита m, така че ако фотон попадне в електрон, енергията му ще бъде погълната и електронът ще се премести на по-висока орбита поради тази допълнителна енергия. Според теорията на Бор, ако електронът падне от по-висока орбита на по-ниска орбита, той ще трябва да отдаде енергия под формата на фотон. Енергията на фотона ще бъде равна на разликата в енергията на двете орбити, а енергията на фотона го кара да има определена честота и цвят. Теорията на Бор дава добро обяснение на много аспекти на субатомните явления, но не успява да даде отговор на въпроса защо всеки от цветовете на светлината, произвеждана от нажежения водород (и от нажежения неон или друг елемент), има собствена яркост и разликите в яркостта са винаги еднакви за всеки елемент.
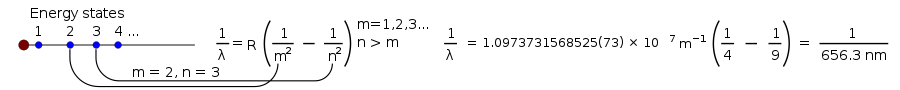
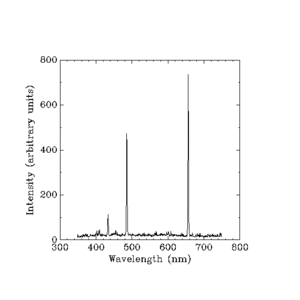
По времето, когато Нилс Бор излага своята теория, повечето неща за светлината, произвеждана от водородна лампа, са известни, но учените все още не могат да обяснят яркостта на всяка от линиите, произвеждани от светещия водород.
Вернер Хайзенберг се заема да обясни яркостта или "интензивността" на всяка линия. Той не можел да използва никакво просто правило като това, което Балмер бил измислил. Трябваше да използва много трудната математика на класическата физика, която изчислява всичко с помощта на неща като масата (теглото) на електрона, заряда (статичната електрическа сила) на електрона и други малки величини. Класическата физика вече имаше отговори за яркостта на цветните ивици, които произвежда водородната лампа, но според класическата теория трябва да има непрекъсната дъга, а не четири отделни цветни ивици. Обяснението на Хайзенберг е:
Има някакъв закон, който казва какви честоти на светлината ще произвежда светещият водород. Той трябва да предсказва отдалечени честоти, когато участващите електрони се движат между орбити близо до ядрото (центъра) на атома, но също така трябва да предсказва, че честотите ще стават все по-близки и по-близки, когато наблюдаваме какво прави електронът, движейки се между орбити все по-далеч и по-далеч. Той също така ще предскаже, че разликите в интензитета на честотите се приближават все повече и повече, докато се отдалечаваме. Там, където класическата физика вече дава правилните отговори чрез един набор от уравнения, новата физика трябва да даде същите отговори, но чрез различни уравнения.
Класическата физика използва математическите методи на Джоузеф Фурие, за да направи математическа картина на физическия свят, Тя използва колекции от гладки криви, които се събират, за да направят една гладка крива, която дава, в този случай, интензитети за светлина на всички честоти от някаква светлина. Но това не е правилно, защото тази гладка крива се появява само при по-високи честоти. При по-ниските честоти винаги има изолирани точки и нищо не свързва точките. Така че, за да направи карта на реалния свят, Хайзенберг е трябвало да направи голяма промяна. Трябвало да направи нещо, за да подбере само числата, които да съответстват на наблюдаваното в природата. Понякога хората казват, че той е "отгатнал" тези уравнения, но той не е правил сляпо предположение. Той е намерил това, което му е било необходимо. Числата, които изчислил, щели да поставят точки върху графиката, но между точките нямало да бъде прокарана линия. А ако направеше една "графика" само от точки за всеки набор от изчисления, щеше да изхарчи много хартия и нямаше да свърши нищо. Хайзенберг намерил начин ефективно да прогнозира интензитетите за различни честоти и да организира тази информация по полезен начин.
Само с помощта на емпиричното правило, дадено по-горе, това, което Балмер започна и Ридберг подобри, можем да видим как да получим един набор от числа, които биха помогнали на Хайзенберг да получи желаната от него картина:
Правилото гласи, че когато електронът преминава от една орбита в друга, той или печели, или губи енергия в зависимост от това дали се отдалечава от центъра, или се приближава към него. Така че можем да поставим тези орбити или енергийни нива като заглавия в горната и страничната част на мрежата. По исторически причини най-ниската орбита се нарича n, а следващата орбита навън се нарича n - a, след това идва n - b и т.н. Объркващо е, че са използвали отрицателни числа, когато електроните всъщност са придобивали енергия, но това е просто така.
Тъй като правилото на Ридберг ни дава честоти, можем да използваме това правило, за да въведем числа в зависимост от това къде отива електронът. Ако електронът започне от n и завърши на n, тогава той всъщност не е отишъл никъде, така че не е спечелил енергия и не е загубил енергия. Така че честотата е 0. Ако електронът започне от n-a и завърши на n, тогава той е паднал от по-висока орбита на по-ниска орбита. Ако това е така, той губи енергия, а загубената енергия се проявява като фотон. Фотонът има определено количество енергия, e, и то е свързано с определена честота f чрез уравнението e = h f. Така че знаем, че определена промяна на орбитата ще доведе до определена честота на светлината, f. Ако електронът започва от n и завършва на n - a, това означава, че е преминал от по-ниска орбита на по-висока. Това се случва само когато фотон с определена честота и енергия дойде отвън, бъде погълнат от електрона и му предаде енергията си, и това е, което кара електрона да излезе на по-висока орбита. За да има смисъл, записваме тази честота като отрицателно число. Имало е фотон с определена честота и сега тя е отнета.
Така че можем да съставим мрежа по следния начин, където f(a←b) означава честотата, която участва, когато електронът преминава от енергийно състояние (орбита) b в енергийно състояние a (Отново, последователностите изглеждат обърнати назад, но това е начинът, по който са били записани първоначално.):
Мрежа на f
| Електронни състояния | n | n-a | n-b | n-c | .... | |
| n | f(n←n) | f(n←n-a) | f(n←n-b) | f(n←n-c) | ..... | |
| n-a | f(n-a←n) | f(n-a←n-a) | f(n-a←n-b) | f(n-a←n-c) | ..... | |
| n-b | f(n-b←n) | f(n-b←n-a) | f(n-b←n-b) | f(n-b←n-c) | ..... | |
| преход.... | ..... | ..... | ..... | ..... | | |
Хайзенберг не е направил решетките по този начин. Той просто е направил математическите изчисления, които са му позволили да получи интензитета, който е търсил. Но за да направи това, той е трябвало да умножи две амплитуди (колко висока е една вълна), за да изчисли интензитета. (В класическата физика интензивността е равна на амплитуда, повдигната на квадрат.) Той съставил странно изглеждащо уравнение, за да се справи с този проблем, написал останалата част от работата си, предал я на шефа си и излязъл в отпуск. Д-р Борн погледнал смешното си уравнение и то му се сторило малко налудничаво. Сигурно се е запитал: "Защо Хайзенберг ми даде това странно нещо? Защо трябва да го направя по този начин?" След това осъзнал, че гледа проект за нещо, което вече познавал много добре. Беше свикнал да нарича решетката или таблицата, която можехме да напишем, правейки например цялата математика за честотите, матрица. А странното уравнение на Хайзенберг беше правило за умножаване на две от тях заедно. Макс Борн беше много, много добър математик. Той знаеше, че тъй като двете матрици (мрежи), които се умножават, представляват различни неща (като позиция (x,y,z) и импулс (mv) например), то когато умножите първата матрица по втората, получавате един отговор, а когато умножите втората матрица по първата, получавате друг отговор. Въпреки че не е знаел нищо за матричната математика, Хайзенберг вече е виждал този проблем с "различните отговори" и той го е притеснявал. Но д-р Борн бил толкова добър математик, че видял, че разликата между умножението на първата и втората матрица винаги ще включва константата на Планк, h, умножена по квадратния корен от отрицателната единица, i. Така че в рамките на няколко дни след откритието на Хайзенберг те вече имали основната математика за това, което Хайзенберг обичал да нарича "принцип на неопределеността". Под "неопределеност" Хайзенберг разбираше, че нещо като електрона просто не може да се определи, докато не се определи. Той е малко като медуза, която винаги се мачка наоколо и не може да бъде "на едно място", докато не я убиете. По-късно хората придобиха навика да го наричат "принципът на неопределеност на Хайзенберг", което накара много хора да направят грешката да мислят, че електроните и подобни неща наистина са "някъде", но ние просто не сме сигурни в това в собственото си съзнание. Тази идея е погрешна. Тя не е това, за което говори Хайзенберг. Да имаш проблеми с измерването на нещо е проблем, но това не е проблемът, за който говори Хайзенберг.
Идеята на Хайзенберг е много трудна за възприемане, но можем да я изясним с един пример. Първо, ще започнем да наричаме тези решетки "матрици", защото скоро ще трябва да говорим за умножение на матрици.
Да предположим, че започваме с два вида измервания - позиция (q) и импулс (p). През 1925 г. Хайзенберг написва уравнение, подобно на това:
Y ( n , n - b ) = ∑ a p ( n , n - a ) q ( n - a , n - b ) {\displaystyle Y(n,n-b)=\sum _{a}^{}\,p(n,n-a)q(n-a,n-b)} (Уравнение за конюгираните променливи импулс и позиция)
(Уравнение за конюгираните променливи импулс и позиция)
Той не е знаел това, но това уравнение дава план за изписване на две матрици (мрежи) и за тяхното умножаване. Правилата за умножаване на една матрица по друга са малко объркани, но ето двете матрици според плана, а след това и тяхното произведение:
Матрица на p
| Електронни състояния | n-a | n-b | n-c | .... | |
| n | p(n←n-a) | p(n←n-b) | p(n←n-c) | ..... | |
| n-a | p(n-a←n-a) | p(n-a←n-b) | p(n-a←n-c) | ..... | |
| n-b | p(n-b←n-a) | p(n-b←n-b) | p(n-b←n-c) | ..... | |
| преход.... | ..... | ..... | ..... | ..... | |
Матрица на q
| Електронни състояния | n-b | n-c | n-d | .... | |
| n-a | q(n-a←n-b) | q(n-a←n-c) | q(n-a←n-d) | ..... | |
| n-b | q(n-b←n-b) | q(n-b←n-c) | q(n-b←n-d) | ..... | |
| n-c | q(n-c←n-b) | q(n-c←n-c) | q(n-c←n-d) | ..... | |
| преход.... | ..... | ..... | ..... | ..... | |
Матрицата за произведението на горните две матрици, както е определено от съответното уравнение в статията на Хайзенберг от 1925 г., е:
| Електронни състояния | n-b | n-c | n-d | ..... |
| n | A | ..... | ..... | ..... |
| n-a | ..... | B | ..... | ..... |
| n-b | ..... | ..... | C | ..... |
Къде:
A=p(n←n-a)*q(n-a←n-b)+p(n←n-b)*q(n-b←n-b)+p(n←n-c)*q(n-c←n-b)+.....
B=p(n-a←n-a)*q(n-a←n-c)+p(n-a←n-b)*q(n-b←n-c)+p(n-a←n-c)*q(n-c←n-c)+.....
C=p(n-b←n-a)*q(n-a←n-d)+p(n-b←n-b)*q(n-b←n-d)+p(n-b←n-c)*q(n-d←n-d)+.....
и т.н.
Ако матриците се обърнат, ще се получат следните стойности:
A=q(n←n-a)*p(n-a←n-b)+q(n←n-b)*p(n-b←n-b)+q(n←n-c)*p(n-c←n-b)+.....
B=q(n-a←n-a)*p(n-a←n-c)+q(n-a←n-b)*p(n-b←n-c)+q(n-a←n-c)*p(n-c←n-c)+.....
C=q(n-b←n-a)*p(n-a←n-d)+q(n-b←n-b)*p(n-b←n-d)+q(n-b←n-c)*p(n-d←n-d)+.....
и т.н.
Обърнете внимание как промяната на реда на умножение променя стъпка по стъпка числата, които действително се умножават.