Реакцията SN 2 (известна също като двумолекулно нуклеофилно заместване) е реакция на заместване в органичната химия. Тя е вид нуклеофилно заместване, при което самотна двойка от нуклеофил атакува електронодефицитен електрофилен център и се свързва с него. По този начин се изхвърля друга група, наречена "напускаща група". Така входящата група замества напускащата група в една стъпка. Тъй като в бавната, определяща скоростта стъпка на реакцията участват два реагиращи вида, това води до наименованието бимолекулярно нуклеофилно заместване или SN 2. Сред неорганичните химици реакцията SN 2 често е известна като механизъм на взаимозамяна.
Основни характеристики и кинетика
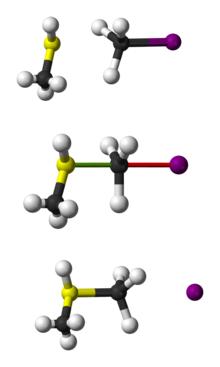
Концертен механизъм: SN2 е концертна (едностъпкова) реакция — образуването на връзка между нуклеофила и въглеродния център и разкъсването на връзката с напускащата група стават едновременно, през преходно състояние.
Законово уравнение за скоростта: скоростта на реакцията следва вторичен порядък и зависи едновременно от концентрациите на субстрата (R–LG) и нуклеофила (Nu): rate = k [R–LG][Nu].
Структура на преходното състояние и стереохимия
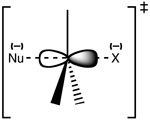
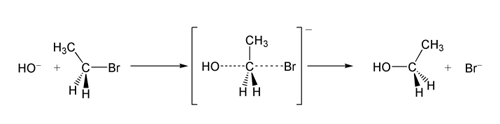
При SN2 нуклеофилът атакува въглеродния атом от страната, противоположна на напускащата група (т.нар. задно или „backside“ нападение). Преходното състояние е петикоординатно, със частично образувана нова връзка и частично нарушена стара връзка — често се описва като тригонална бипирамидална геометрия с удължени връзки.
Инверсия на Валенда (Walden inversion): резултатът от задното нападение е инвертирана абсолютна конфигурация на централния въглерод (R ↔ S). Това е характерна стереохимична следа за механизма SN2.
Фактори, които ускоряват или забавят SN2
- Субстрат (стеричност): реактивността следва общо порядък: метил > първичен > вторичен >> третичен (третични алкилхалиди почти не протичат по SN2 поради стерично отблъскване).
- Нуклеофил: по-силните нуклеофили (обикновено по-заредени и по-малко електроотрицателни) ускоряват SN2. Примери: OH–, CN–, RS–. Поляризуемостта също повлиява — големи, поляризуеми йони са добри нуклеофили в полярни протични среди.
- Напускаща група: по-добри напускащи групи ускоряват реакцията (I– > Br– > Cl– >> F–). Стабилността на оставения анион е важна.
- Разтворител: полярни апроти́чни разтворители (напр. DMSO, DMF, ацетон) благоприятстват SN2, тъй като не солватират силно нуклеофилите и те остават „активни“. Полярните протични (напр. H2O, спиртове) солватират и отслабват нуклеофила, което забавя реакцията.
- Електронни ефекти и съседни групи: бензилови и аллилни центрове често ускоряват SN2 поради делокализация на заряда в преходното състояние. Също така участие на съседни групи (neighboring group participation) може да промени механизма.
Конкуриращи процеси
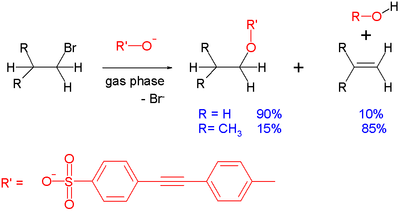
При вторични и особено при третични субстрати често се получава конкуренция между SN2 и елиминиране E2. Силни, големи бази (напр. t-BuO–) предпочитат E2; по-малки, силни нуклеофили (напр. OH–, alkoxidi) могат да дават смес от продукти в зависимост от условията (температура, разтворител).
Примери и практическо приложение
- Класически пример: CH3Br + OH– → CH3OH + Br– — бърза SN2 реакция с инверсия (за метилови съединения няма стереохимичен въпрос).
- Заместителни реакции при синтез: SN2 се използва за въвеждане на нуклеофилни групи (алкохолати → етери, цианиди → нитрилни групи и т.н.).
- Арили и винилни халогениди обикновено не реагират по SN2, защото целевият въглерод е sp2-гибридизиран и достъпът за задно нападение е блокиран.
Енергетична диаграма (интуитивно)
В типичната енергетична профилна крива SN2 има една енергийна бариера (преходно състояние) между реагентите и продуктите. Енергията на активация зависи от описаните фактори (стеричност, нуклеофил, напускаща група, разтворител).
Кратки практически съвети за лабораторен синтез
- За да насърчите SN2: използвайте метилови или първични халогениди, силен нуклеофил и полярен апротичен разтворител.
- Ако наблюдавате голямо количество елиминация (E2), опитайте да намалите температурата, да смените разтворителя или да използвате по-слаб, но по-специфичен нуклеофил.
Обобщено: SN2 е бърз, едностъпков механизъм на нуклеофилно заместване с характерна инверсия на конфигурацията и ясно зависим от стеричните и електронните свойства на реагентите и разтворителя. Познаването на тези фактори позволява да се планират и оптимизират реакции в органичния синтез.