Молекулна орбитала: определение, модели и роля в квантовата химия
Молекулна орбитала: ясно определение, моделни подходи и роля в квантовата химия, визуални обяснения и практични примери за студенти и изследователи
В химията молекулната орбитала (или MO) обяснява какво се случва с електроните, когато атомите се съединяват в молекула. МО е математическа функция, която описва вълновото поведение на електрона в молекулата. Функциите могат да кажат каква е вероятността да се намери електрон в определена област. Химиците използват такива функции, за да предскажат или обяснят химични и физични свойства.
Химиците обикновено изграждат математически модели на молекулни орбитали чрез комбиниране на атомни орбитали. Могат да се използват и хибридни орбитали от всеки атом на молекулата или други молекулни орбитали от групи атоми. Компютрите могат да работят с тези функции. Молекулните орбитали позволяват на химиците да прилагат квантовата механика за изучаване на молекулите. МО отговарят на въпроси за това как атомите в молекулите се придържат един към друг. Различните закръглени форми в орбиталната диаграма показват къде най-вероятно ще се намират електроните в един атом.
Какво означава това на практика
Молекулната орбитала не е „малка кълбичка“, а математическа вълнова функция, чийто квадрат описва вероятността да намерим електрон в дадена точка около молекулата. Когато атомни орбитали се припокриват, комбинацията им може да образува орбитали с по-висока или по-ниска енергия спрямо изходните атомни орбитали.
Основни модели и понятия
- LCAO (Linear Combination of Atomic Orbitals) — най-често използваният подход: молекулната орбитала се описва като линейна комбинация от атомни орбитали. Този метод дава ясна представа за това кои атоми „участват“ в дадена МО.
- Свързващи и анти-свързващи орбитали — при конструкция на МО се получават орбитали с повишена (анти-свързващи) или понижена (свързващи) енергия спрямо изходните атомни орбитали. Запълването на свързващи орбитали стабилизира молекулата, докато запълването на анти-свързващи я дестабилизира.
- HOMO и LUMO — най-високоенергийната запълнена орбитала (HOMO) и най-нискоенергийната празна орбитала (LUMO) са ключови за обяснение на химичната реактивност: разликата им (енергийна празнина) влияе върху оптичните и електронните свойства.
- Август-Полициклични правила — при по-сложни молекули симетрията и разпределението на орбиталите определят понятия като ароматичност и антиароматичност.
Как се изчисляват молекулните орбитали
В практиката се използват различни квантово-химични методи:
- Хартри–Фок (HF) — основен метод, който дава описания на еднаелектронни орбитали, но пренебрегва пълното корелиране на електроните.
- Методи за корелация (например MP2, CI, CCSD) — добавят ефекти на взаимодействие между електроните и повишават точността.
- Плътностно-функционална теория (DFT) — балансира скорост и точност и е широко използвана за по-големи системи.
Изборът на базисни функции (basis set) и ниво на теория влияе силно на формата и енергията на МО, затова при резултати трябва да се посочват използваните методи и параметри.
Приложения и значение
- Предсказване на реактивност — чрез анализ на HOMO/LUMO и разпределение на електронната плътност могат да се определят сайтове за атака в органични реакции.
- Спектроскопия — МО описват електронните преходи (например UV–vis), както и резултатите от фотоелектронна спектроскопия (информация за енергията на запълнените орбитали).
- Материални свойства — проводимост, магнитни свойства и фотофизични характеристики зависят от структурата на молекулните орбитали в твърди вещества и молекулни материали.
- Катализ и дизайн на лекарства — знанието за МО помага при проектиране на каталитични центрове и взаимодействия между лиганди и биомолекули.
Практически изобразяване
Молекулните орбитали често се визуализират чрез изосурфейси (повърхности с еднаква плътност на вълновата функция). Цветовете/знакът показват фазата на вълновата функция, което е важно при разглеждане на интерференция (конструкция/деструкция) между орбиталите.
Ограничения и предупреждения
- МО са резултат от модели и приближения — точността зависи от избрания метод и базис.
- Електронната корелация понякога е силно въздействаща и изисква по-сложни методи за точно прогнозиране.
- Интерпретацията на МО трябва да се прави внимателно: различни представяния (например локализирани срещу делокализирани орбитали) са полезни за различни цели, но не са „абсолютни истини“.
Кратко резюме
Молекулните орбитали са фундаментален инструмент в съвременната химия: чрез тях се прилага квантовата механика за обяснение и предсказване на структура, реактивност и свойства на молекулите. Комбинирайки теория и компютърно моделиране, химиците получават практични прозрения, които водят до открития в синтез, материалознание и биохимия.
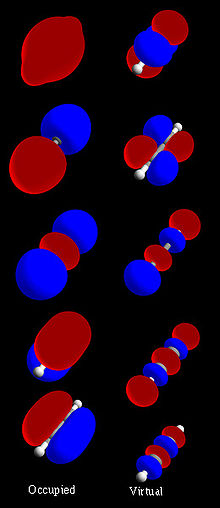
Фигура 1: Пълен набор от молекулни орбитали на ацетилена (H-C≡C-H)
История
Думата "орбитален" е използвана за първи път на английски език от Робърт С. Мъликен. Немският физик Ервин Шрьодингер пише за орбитите по-рано. Шрьодингер ги нарича Eigenfunktion.
През 1926 г. физикът Макс Борн описва теорията за молекулните орбитали. Днес тя е известна като правилото на Борн и е част от Копенхагенската интерпретация на квантовата механика. Когато е предложена първоначално, тази теория не съвпада с модела на атома на Нилс Бор. Моделът на Бор описва електроните като "обикалящи" около ядрото, като се движат в кръг. В крайна сметка обаче моделът на Борн получава популярна подкрепа, тъй като успява да опише разположението на електроните в молекулите и обяснява редица необясними дотогава химични реакции.
Преглед
Атомните орбитали предсказват позицията на електрона в атома. Молекулните орбитали се създават, когато атомните орбитали се обединят. Молекулната орбитала може да даде информация за електронната конфигурация на молекулата. Електронната конфигурация е най-вероятната позиция и енергията на един (или една двойка) електрон(и). В повечето случаи МО се представя като линейна комбинация от атомни орбитали (методът LCAO-MO), особено при приблизителна употреба. Това означава, че химиците приемат, че вероятността електронът да се намира в която и да е точка на молекулата е сумата от вероятностите електронът да се намира там въз основа на отделните атомни орбитали. LCAO-MO е прост модел на връзката в молекулите и е важен за изучаването на теорията на молекулните орбитали.
Теоретичните химици използват компютри, за да изчислят МО на различни молекули (както реални, така и въображаеми). Компютърът може да начертае графики на "облака", за да покаже колко вероятно е електронът да се намира във всяка област. Компютрите могат да дадат информация и за физичните свойства на молекулата. Могат също така да кажат колко енергия е необходима за образуването на молекулата. Това помага на химиците да кажат дали някои малки молекули могат да се комбинират, за да се получат по-големи молекули.
Повечето съвременни методи за изчислителна химия започват с изчисляване на МО на дадена система. Електрическото поле на всеки МО се генерира от ядрата на всички атоми и някакво средно разпределение на другите електрони.
Аналогия
Разбирането на МО е подобно на задачата да се разбере къде се намира всеки служител в голям магазин за домашни потреби (без да се гледа вътре в магазина). Анализаторът знае броя на служителите, работещи в магазина, и отдела на всеки служител. Той също така знае, че служителите не си стъпват на краката и че служителите стоят в коридора, а не на рафтовете със стоки. Служителите напускат собствения си отдел, за да помогнат на клиентите да намерят стоките в други отдели или да проверят наличностите. Анализаторът, който дава местоположението на всички служители в магазина в избран момент, без да погледне вътре, е като химик, който изчислява МО на молекула. Точно както МО не могат да определят точното местоположение на всеки електрон, така и точното местоположение на всеки служител не е известно. МО, който има възлова равнина, е като заключението, че служителите се разхождат по коридорите, а не по рафтовете. Въпреки че електроните се внасят от определен атом, електронът запълва МО без оглед на неговия атомен източник. Това е като служител, който през деня напуска своя отдел, за да се разхожда на друго място в магазина. Така че МО е непълно описание на електрона, точно както изчисленията на анализатора за невидимия магазин са непълно предположение за местоположението на служителите.

Изчисляването на МО е като предвиждане на местоположението на всеки служител в магазин за домашни потреби.
Образуване на молекулни орбитали
Теоретичните химици са измислили правила за изчисляване на МО. Тези правила произтичат от разбирането на квантовата механика. Квантовата механика помага на химиците да използват казаното от физиката за електроните, за да разберат как се държат електроните в молекулите. Молекулните орбитали се формират от "позволени" взаимодействия между атомните орбитали. (Взаимодействията са "разрешени", ако симетриите (определени от теорията на групите) на атомните орбитали са съвместими помежду си.) Химиците изучават взаимодействията между атомните орбитали. Тези взаимодействия са резултат от припокриването (мярка за това колко добре две орбитали конструктивно взаимодействат помежду си) между две атомни орбитали. Припокриването е важно, ако атомните орбитали са близки по енергия. И накрая, броят на МО в молекулата трябва да е равен на броя на атомните орбитали в атомите, които се обединяват, за да образуват молекулата.
Качествен подход
Химиците трябва да разбират геометрията на МО, за да обсъждат молекулната структура. Методът LCMO (Linear combination of atomic orbitals molecular orbital) дава грубо, но добро описание на МО. При този метод молекулните орбитали се изразяват като линейни комбинации на всички атомни орбитали на всеки атом в молекулата.
Линейни комбинации на атомни орбитали (LCAO)
Молекулните орбитали са въведени за първи път от Фридрих Хунд и Робърт С. Мъликен през 1927 и 1928 г.
Линейната комбинация от атомни орбитали или "LCAO" приближението за молекулните орбитали е въведено през 1929 г. от сър Джон Ленард-Джоунс. Неговата новаторска статия показва как да се изведе електронната структура на молекулите на флуора и кислорода от квантовите принципи. Този качествен подход към теорията на молекулните орбитали е част от началото на съвременната квантова химия.
Линейните комбинации на атомните орбитали (LCAO) могат да се използват, за да се предположат молекулните орбитали, които се образуват, когато атомите на молекулата се свържат помежду си. Подобно на атомната орбитала, уравнението на Шрьодингер, което описва поведението на електрона, може да се построи и за молекулна орбитала. Линейните комбинации на атомните орбитали (сумите и разликите на атомните вълнови функции) дават приблизителни решения на молекулните уравнения на Шрьодингер. За прости двуатомни молекули получените вълнови функции се представят математически чрез уравненията
Ψ = ca ψa + cb ψb
и
Ψ* = ca ψa - cb ψb
където Ψ и Ψ* са молекулните вълнови функции съответно за свързващата и антисвързващата молекулна орбитала, ψa и ψb са атомните вълнови функции съответно от атоми a и b, а ca и cb са регулируеми коефициенти. Тези коефициенти могат да бъдат положителни или отрицателни в зависимост от енергиите и симетриите на отделните атомни орбитали. С приближаването на двата атома атомните им орбитали се припокриват и се получават области с висока електронна плътност. Така между двата атома се образуват молекулни орбитали. Атомите се държат заедно чрез електростатичното привличане между положително заредените ядра и отрицателно заредените електрони, заемащи свързващите молекулни орбитали.
Свързващи, антисвързващи и несвързващи МО
Когато атомните орбитали взаимодействат, получената молекулна орбитала може да бъде три вида: свързваща, антисвързваща или несвързваща.
Мотиви за свързване:
- Взаимодействията между атомните орбитали са конструктивни (вътрефазни) взаимодействия.
- Свързващите МО са с по-ниска енергия от атомните орбитали, които се комбинират, за да ги създадат.
Антисвързващи МО:
- Антисвързващите взаимодействия между атомните орбитали са деструктивни (извънфазови) взаимодействия.
- Антисвързващите МО са с по-висока енергия от атомните орбитали, които се комбинират, за да ги създадат.
Несвързващи МО:
- Несвързаните МО са резултат от липсата на взаимодействие между атомните орбитали поради липсата на съвместими симетрии.
- Несвързаните МО ще имат същата енергия като атомните орбитали на един от атомите в молекулата.
HOMO и LUMO
Всяка молекулна орбитала има свое собствено енергийно ниво. Химиците подреждат МО по енергийни нива. Химиците предполагат, че електроните първо ще запълнят МО с най-ниско енергийно ниво. Например, ако една молекула има електрони за запълване на 15 орбитали, ще бъдат запълнени 15-те МО с най-ниски енергийни нива. Петнадесетата МО в списъка ще се нарича "най-високо заета молекулна орбитала" (HOMO), а шестнадесетата МО в списъка ще бъде "най-ниско незаета молекулна орбитала" (LUMO). Разликата между енергийното ниво на HOMO и енергийното ниво на LUMO се нарича лентова междина. Понякога лентовата разлика може да служи като мярка за възбудимостта на молекулата: колкото по-малка е енергията, толкова по-лесно ще бъде възбудена. Когато електронът е възбуден, той ще премине в незаета МО. Например това може да помогне да се предположи дали нещо ще излъчва светлина (луминесценция).
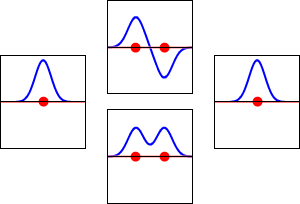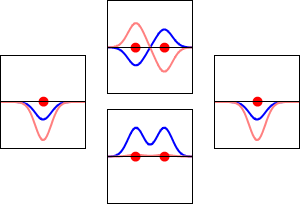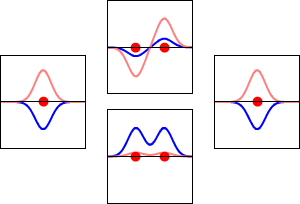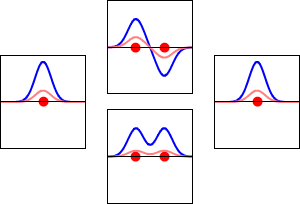
Електронни вълнови функции за орбитала 1s на водородния атом (вляво и вдясно) и съответните свързващи (долу) и антисвързващи (горе) молекулни орбитали на молекулата H2 . Реалната част на вълновата функция е синята крива, а въображаемата част е червената крива. С червените точки са отбелязани местата на протоните. Електронната вълнова функция осцилира в съответствие с вълновото уравнение на Шрьодингер, а орбиталите са нейните стоящи вълни. Честотата на стоящата вълна е пропорционална на енергията на орбитата. (Тази графика е едноизмерен разрез на триизмерната система.)
Въпроси и отговори
В: Какво представлява молекулната орбитала?
О: Молекулна орбитала (или МО) е математическа функция, която описва вълновото поведение на електрона в молекула. Тя обяснява какво се случва с електроните, когато атомите се съединяват в молекула, и може да определи вероятността за намиране на електрон във всяка конкретна област.
Въпрос: Как химиците изграждат математически модели на молекулните орбитали?
О: Химиците обикновено изграждат математически модели на молекулни орбитали, като комбинират атомни орбитали. Могат да се използват и хибридни орбитали от всеки атом на молекулата или други молекулни орбитали от групи атоми. Компютрите могат да работят с тези функции.
Въпрос: Какво общо има квантовата механика с изучаването на молекулите?
О: Молекулните орбитали позволяват на химиците да прилагат квантовата механика за изучаване на молекулите. Те дават отговор на въпроси за това как атомите в молекулите се придържат един към друг и дават представа за химичните и физичните свойства.
В: Какво представляват орбиталните диаграми?
О: Орбиталните диаграми са визуални изображения, които показват къде най-вероятно ще се намират електроните в даден атом въз основа на различните му заоблени форми.
В: Как работят хибридните орбитали?
О: Хибридните орбитали комбинират различни видове атомни орбити в един нов вид, който има уникални характеристики в сравнение с компонентите си. Тези хибриди често се използват при изграждането на математически модели за молекулни орбитали.
В: Как компютрите могат да помогнат при изучаването на МО?
О: Компютрите могат да помогнат при изучаването на МО, като работят върху техните функции и предоставят по-точни прогнози или обяснения за химичните и физичните свойства в молекулите.
обискирам