Реакция на Гриняр – механизъм, приложения и приготвяне на реагенти
Реакция на Гриняр: подробен механизъм, практични приложения и безопасно приготвяне на реагенти – ръководство за химици, студенти и изследователи.
Реакцията на Гриняр (произнася се /ɡriɲar/) е органометална химична реакция, при която алкил- или арил-магнезиеви халогениди (наричани реагенти на Гриняр) атакуват електрофилни въглеродни атоми, най-често такива, участващи в полярни връзки (например в карбонилна група). Реагентите на Гриняр действат като нуклеофили и позволяват образуването на нови връзки въглерод–въглерод, като променят хибридизацията в реакционния център. Освен това могат да се използват за формиране на връзки въглерод–фосфор, въглерод–олово, въглерод–силиций, въглерод–борон и други въглерод–хетероатомни връзки.
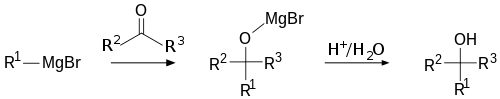
Механизъм (обща представа)
Общата стъпка при атакуване на карбонил от реагент на Гриняр (RMgX) е нуклеофилно присъединяване към карбонилния въглерод, образувайки алкоксиден интермедиат, който при киселинно последващо обработване дава съответния алкохол. Поради високата основност на алкилната част (пKa на алканите ~45), реагентът показва силно нуклеофилно и основно поведение: често първо ще депротонира всяка налична киселинна група, преди да атакува електрофила.
Иницирането на формирането на RMgX от R–X и Mg обикновено включва едноелектронни трансферни стъпки и образуване на радикални/радикално-анионни интермедиати; в готов вид реагентът не е просто свободен йон, а съществува като агрегати/клъстери, стабилизирани чрез координация към етерни молекули. Поради това е по-паметно да се каже, че реакциите на Гриняр не са „чисто йонни“ в класическия смисъл.
Общи приложения
- Добавяне към алдехиди и кетони дава съответно вторични и третични алкохоли (след киселинно work-up).
- Реакция с естери често дава третични алкохоли (посредством двукратно присъединяване).
- Реакция с CO2 дава карбоксилна киселина след киселинно обработване.
- Реакция с нитрилни групи води до кетони след хидролиза на иминовия интермедиат.
- Отваряне на епоксиди при по-малко субституирания въглерод дава алкохоли с удължена въглеродна верига.
- В органична синтеза RMgX се използват и за трансметалации (за образуване на връзки C–Si, C–B и др.) и като междинен инструмент при сложни многостъпкови синтези.
Приготвяне на реагенти на Гриняр
Най-разпространеният начин за приготвяне е директно от алкил- или арил-халогенид и метален магнезий в сухи етери (типично диетилов етер или THF). Общият процес:
- Смесват се R–X и чист магнезий в сух разтворител при инертна атмосфера (азот или аргон).
- За активиране на повърхността на Mg често се използват методи като механично разбъркване, нагряване, добавяне на няколко капки йод или 1,2-диброметан, или ултразвукова активация. Това помага да се преодолее пасивния оксиден слой на Mg и да започне реакцията.
- Йодидите реагират най-лесно, следвани от бромиди; хлоридите обикновено са най-малко реактивни и при някои случаи се използват каталитични/специални процедури или активирани форми на Mg.
Практически съображения и ограничения
Анаеробни и анхидридни условия: Реагентите на Гриняр са изключително чувствителни към влага и киселинни протони — реагират бързо с вода, алкохоли, амини или други протонни донори, което унищожава активния реагент. Затова е задължително използване на изсушена посуда, сухи разтворители и инертна атмосфера.
Активиране и чистота: Атмосферната влага и органични примеси влияят на добива при директно получаване от магнезиеви стружки. Освен фламбеленo изсушаване на стъкления съд, химиците използват ултразвук и други активиращи методи, за да подобрят повърхностната реактивност на Mg и да намалят чувствителността към остатъчна вода.
Странични реакции и ограничения: RMgX могат да реагират с други електрофилни центрове или да дават елиминация/вюртц-подобни странични продукти при определени субстрати. Те не са надежден метод за директно създаване на въглерод–въглерод връзки чрез нуклеофилно заместване на алкилхалогениди (реакция по механизма S 2. N), тъй като RMgX предпочитат да се държат като силна основа/нуклеофил по други пътища.
Безопасност и работа с реагента
- Използвайте сухи разтворители и работете под инертен газ (N2/Ar).
- Носете подходящи лични предпазни средства — очила, ръкавици и лабораторна престилка.
- При смесване или приготвяне може да има екзотермични ефекти; контролирайте температурата и добавяйте реагентите бавно при нужда.
- Крайното ‘загасване’ (quench) се извършва внимателно, обикновено чрез бавно добавяне на разреден воден разтвор (напр. сатуриран NH4Cl или разредена киселина) при охлаждане, за да се избегнат бурни реакции и пръски.
Историческа бележка
Реакциите и реагентите носят името на френския химик Франсоа Огюст Виктор Гриняр, който ги открива и за тази работа получава Нобелова награда за химия през 1912 г.
Кратко резюме: Реакцията на Гриняр е мощен и широко използван инструмент в органичния синтез за формиране на въглерод–въглерод връзки и за въвеждане/трансформиране на различни функционални групи. Успехът ѝ зависи от сухи условия, подходяща активация на магнезия и внимателно управление на реакционните условия.

Разтвор на карбонилно съединение се добавя към реактив на Гриняр. (Вижте галерията по-долу)
Механизъм на реакцията
Прибавянето на Гринярдовия реагент към карбонил обикновено преминава през преходно състояние на шестчленен пръстен.
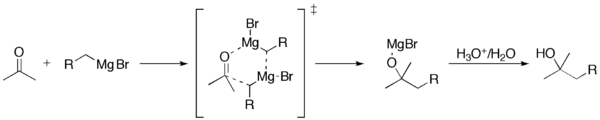
Въпреки това при стерилно възпрепятствани реагенти на Гриняр реакцията може да протече чрез пренос на един електрон.
Реакциите на Гриняр не протичат при наличие на вода; водата води до бързо разлагане на реактива. Затова повечето реакции на Гриняр протичат в разтворители като безводен диетилов етер или тетрахидрофуран (THF), тъй като кислородът в тези разтворители стабилизира магнезиевия реагент. Реагентът може да реагира и с кислорода, който се съдържа в атмосферата. При това между въглеродната основа и групата на магнезиевия халогенид се вмъква кислороден атом. Обикновено тази странична реакция може да бъде ограничена от изпаренията на летливите разтворители, които изместват въздуха над реакционната смес. Химиците обаче могат да извършват реакциите в азотна или аргонова атмосфера. При реакциите в малък мащаб парите на разтворителя нямат достатъчно пространство, за да предпазят магнезия от кислорода.
Създаване на реагент на Гриняр
Реагентите на Гриняр се образуват от действието на алкилен или арилен халогенид върху магнезиев метал. Реакцията се провежда чрез добавяне на органичния халогенид към суспензия на магнезий в етер, което осигурява лиганди, необходими за стабилизиране на органомагнезиевото съединение. Типични разтворители са диетилов етер и тетрахидрофуран. Кислородът и протичните разтворители, като вода или алкохоли, не са съвместими с реагентите на Гринярд. Реакцията протича чрез единичен електронен пренос.
R-X + Mg → R-X•− + Mg•+
R-X•− → R• + X−
X− + Mg•+ → XMg•
R• + XMg• → RMgX
Реакциите на Гринярд често започват бавно. Първо, има индукционен период, през който реактивният магнезий се излага на въздействието на органичните реагенти. След този индукционен период реакциите могат да бъдат силно екзотермични. Обичайни субстрати са алкилни и арилбромиди и йодиди. Използват се и хлориди, но флуоридите обикновено са нереактивни, с изключение на специално активирания магнезий, като например магнезия на Рике.
Много от реагентите на Гриняр, като метилмагнезиев хлорид, фенилмагнезиев бромид и алилмагнезиев бромид, се предлагат в търговската мрежа в разтвори на тетрахидрофуран или диетилов етер.
Използвайки равновесието на Шленк, реагентите на Гриняр образуват различни количества диорганмагнезиеви съединения (R = органична група, X = халогенид):
2 RMgX R![]() 2 Mg + MgX2
2 Mg + MgX2
Иницииране
Разработени са много методи за иницииране на реакции на Гринярд, които започват бавно. Тези методи отслабват слоя MgO, който покрива магнезия. Те излагат магнезия на въздействието на органичния халогенид, за да започне реакцията, при която се получава реагентът на Гриняр.
Механичните методи включват раздробяване на парчетата Mg на място, бързо разбъркване или използване на ултразвук (сониране) на суспензията. Обикновено се използват йод, метил йодид и 1,2-диброметотан като активиращи агенти. Химиците използват 1,2-диброметан, тъй като действието му може да се контролира чрез наблюдение на мехурчета етилен. Освен това страничните продукти са безвредни:
Mg + BrC H24 Br → C H24 + MgBr2
Количеството Mg, което се консумира от тези активиращи агенти, обикновено е незначително.
Добавянето на малко количество живачен хлорид ще амалгамира повърхността на метала и ще му позволи да реагира.
Индустриално производство
Реагентите на Гриняр се произвеждат в промишлеността за използване на място или за продажба. Както и при бенчмаркинга, основният проблем е свързан с инициирането. Като инициатор често се използва част от предишна партида от реагента на Гриняр. Реакциите на Гриняр са екзотермични; тази екзотермичност трябва да се вземе предвид, когато реакцията се увеличава от лаборатория до производствено предприятие.
Реакции на реагентите на Гриняр
Реакции с карбонилни съединения
Реагентите на Гриняр ще реагират с различни карбонилни производни.
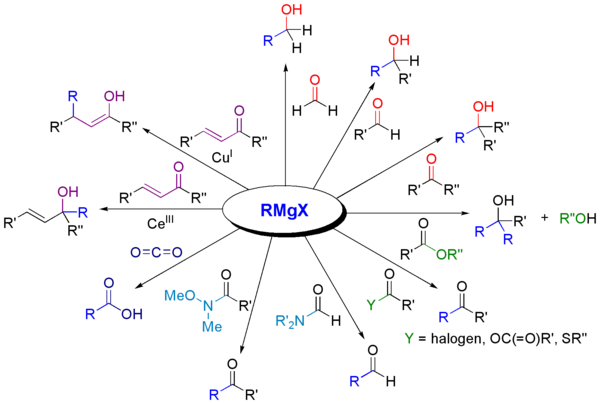
Най-често срещаното приложение е за алкилиране на алдехиди и кетони, както в този пример:
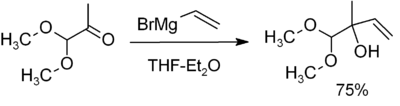
Обърнете внимание, че ацеталната функция (маскиран карбонил) не реагира.
Такива реакции обикновено включват киселинна обработка на водна основа, въпреки че това рядко се показва в реакционните схеми. В случаите, когато реагентът на Гриняр се добавя към прохирален алдехид или кетон, моделът на Фелкин-Ан или правилото на Крам обикновено могат да предскажат кой стереоизомер ще се образува.
Реакции с други електрофили
Освен това реагентите на Гриняр ще реагират с електрофили.
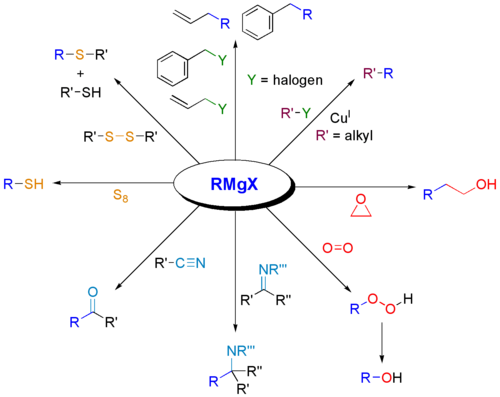
Друг пример е производството на салицилалдехид (не е показан по-горе). Първо, бромоетанът реагира с Mg в етер. Второ, фенол в THF превръща фенола в Ar-OMgBr. Трето, добавя се бензен в присъствието на параформалдехид на прах и триетиламин. Четвърто, сместа се дестилира, за да се отстранят разтворителите. След това се добавя 10 % HCl. Салицилалдехидът ще бъде основният продукт, стига всичко да е много сухо и при инертни условия. Реакцията протича и с йодоетан вместо бромоетан.
Образуване на връзки с B, Si, P, Sn
Реагентът на Гриняр е много полезен за образуване на връзки между въглерод и хетероатом.
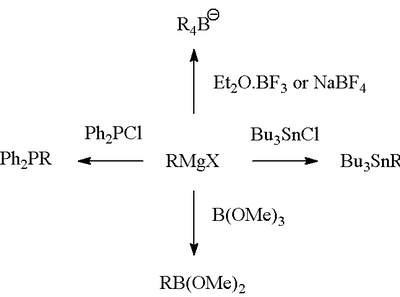
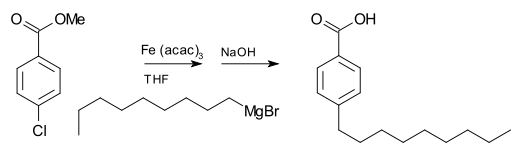
Реакции на свързване въглерод-въглерод
Реагентът на Гринярд може да участва и в реакциите на свързване. Например, нонилмагнезиев бромид реагира с метил р-хлоробензоат, за да се получи р-нонилбензоена киселина в присъствието на трис(ацетилацетонато)желязо(III), често символизирано като Fe(acac)3 , след обработка с NaOH за хидролизиране на естера, показано по следния начин. Без Fe(acac)3 , реагентът на Гриняр би атакувал естерната група над арилхалогенида.
За свързването на арилхалогениди с арилгригнарди никеловият хлорид в тетрахидрофуран (THF) също е добър катализатор. Освен това ефективен катализатор за свързване на алкилни халогениди е дилитиев тетрахлорокупрат (Li2 CuCl4 ), получен чрез смесване на литиев хлорид (LiCl) и меден(II) хлорид (CuCl2 ) в THF. Свързването на Kumada-Corriu дава достъп до [заместени] стирени.
Окисляване
Окислението на реагент на Гриняр с кислород се извършва чрез междинен радикал до магнезиев хидропероксид. При хидролизата на този комплекс се получават хидропероксиди, а при редукцията с допълнителен еквивалент на Григнардовия реактив се получава алкохол.
Реакцията на Григнард с кислород в присъствието на алкен води до получаване на етиленов алкохол. Те са полезни при синтеза на по-големи съединения. Тази модификация изисква арилни или винилни григнардови реагенти. Добавянето само на григнард и алкен не води до реакция, което показва, че присъствието на кислород е от съществено значение. Единственият недостатък е изискването за поне два еквивалента на Григнардовия реагент в реакцията. Този проблем може да се реши чрез използване на двойна система на Гриняр с евтин редуциращ реагент на Гриняр, като например n-бутилмагнезиев бромид.
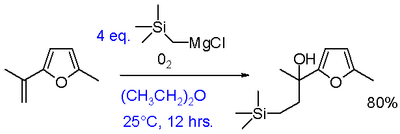
Нуклеофилно алифатно заместване
Реагентите на Гриняр са нуклеофили в нуклеофилните алифатни замествания, например с алкилхалогениди в ключов етап от промишленото производство на напроксен:
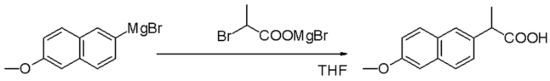
Елиминиране
При синтеза на олефини по Боорд добавянето на магнезий към някои β-халогени води до реакция на елиминиране на алкена. Тази реакция може да ограничи полезността на реакциите на Гриняр.
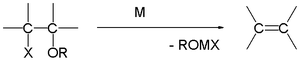
Разграждане на Гриняр
Едно време разграждането на Гриняр е било инструмент за идентифициране (изясняване) на структурата, при което Гриняр RMgBr, образуван от хетероарилбромид HetBr, реагира с вода до Het-H (бром, заменен с водороден атом) и MgBrOH. Този метод на хидролиза позволява да се определи броят на халогенните атоми в дадено органично съединение. В съвременната употреба разграждането на Гриняр се използва при химичния анализ на някои триацилглицероли.
Промишлена употреба
Пример за реакция на Гринярд е ключов етап в промишленото производство на тамоксифен. (Понастоящем тамоксифенът се използва за лечение на рак на гърдата при жени с положителни естрогенни рецептори):
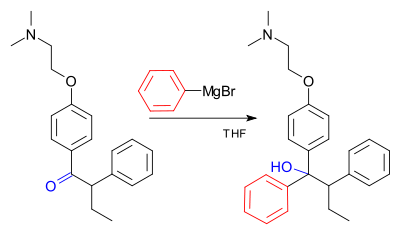
Галерия
· 
Магнезиеви стружки, поставени върху колба.
· 
Покрива се с THF и се добавя малко парченце йод.
· 
При нагряване се добавя разтвор на алкилбромид.
· 
След приключване на добавянето сместа се загрява за известно време.
· 
Образуването на реагента на Гриняр е приключило. В колбата все още остава малко количество магнезий.
· 
Така приготвеният реагент на Гриняр се охлажда до 0°C преди добавянето на карбонилно съединение. Разтворът става мътен, тъй като реагентът на Гриняр се утаява.
· 
Към реактива на Гриняр се добавя разтвор на карбонилно съединение.
· 
Разтворът се загрява до стайна температура. Реакцията е завършена.
Свързани страници
- Реакция на Wittig
- Реакция на Барбие
- Синтез на алдехида Bodroux-Chichibabin
- Реакция на Фуджимото-Бело
- Органолитиеви реактиви
- Реакция на Сакурай
Въпроси и отговори
В: Какво представлява реакцията на Гриняр?
О: Реакцията на Гриняр е органометална химична реакция, при която алкил- или арил-магнезиеви халогениди (реагенти на Гриняр) атакуват електрофилни въглеродни атоми, които се намират в полярни връзки.
Въпрос: Какъв тип връзка се получава при реакцията на Гриняр?
О: Реакцията на Гриняр създава връзка въглерод-въглерод.
В: Какви други видове връзки могат да се образуват чрез реакцията на Гриняр?
О: Реакцията на Гриняр може да образува също така връзки въглерод-фосфор, въглерод-олово, въглерод-силиций, въглерод-бор и други връзки въглерод-хетероатом.
В: Как високата стойност на pKa на алкилния компонент влияе на реакцията на Гринярд?
О: Високата стойност на pKa на алкилния компонент (pKa = ~45) прави реакцията необратима.
В: В какъв тип реакции на добавяне участват реагентите на Гриняр?
О: Реагентите на Гриняр участват в реакции на нуклеофилно органометално присъединяване.
В: Кои са някои недостатъци, свързани с използването на реагентите на Гриняр? О: Някои недостатъци, свързани с използването на реагентите на Гриняр, включват тяхната реактивност с протични разтворители, като вода и функционални групи с кисели протони, като алкохоли и амини; чувствителност към атмосферната влажност; и трудности при образуването на връзки въглерод-въглерод чрез реакция с алкил халогениди по SN2 механизъм.
Въпрос: Кой открива реакцията на Григанд и реагентите?
О: Откриването на реакцията и реагента на Гринд се приписва на френския химик Франсоа Огюст Виктор Гринд, който е удостоен с Нобелова награда за химия през 1912 г. за тази работа.
обискирам
