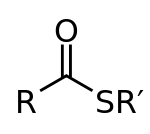
Тиоестерът е молекула с група C-S-CO-C. Те са като естерите, но със серен атом вместо кислороден. Подобно на естерите, те могат да се получат от карбоксилни киселини. При синтеза вместо алкохол се използва тиол.
Тиоестерите са много важни в биохимията. Те се образуват в организма по време на реакциите, при които се получават мастни киселини. Те са също така важни междинни продукти при производството на АТФ, молекулата, която дава енергия на организма.
В химията тиоестерите могат да се използват и като електрофили. Те са по-реактивни от естерите и амидите. Те могат да извършват и алдолни реакции.
Структура и основни свойства
По-общо формулно представяне на тиоестер е R-C(=O)-S-R'. Връзката C=O е аналогична на тази в обикновените естери, но замяната на кислорода с повече поляризиран и по-голям серен атом променя електронното разпределение около карбонилния въглерод. В резултат карбонилният въглерод на тиоестера е по-електрофилен в сравнение с естерите — резонансното делокализиране от S към C=O е по-слабо в сравнение с O, поради по-добрата поляризируемост и по-лошо припокриване на 3p орбиталите на S с 2p орбиталите на въглерода.
Синтез (лаборатория и биосинтеза)
Често използвани лабораторни методи за получаване на тиоестери включват директна кондензация на активирани киселинни производни (като ацилхлориди или активирани естери) с тиоли, или активиране на карбоксилна група чрез карбодиимидазни реагенти (например DCC/EDC) в присъствие на база/катализатор. В биологични системи тиоестери се образуват чрез ензиматично активиране на карбоксилни киселини — класически пример е свързването на ацетилната група с тиолната група на коензим A (CoA), образувайки ацетил-CoA.
Биохимична роля и примери
Някои от най-важните биомолекули, съдържащи тиоестерни връзки, са ацетил-CoA, сукцинил-CoA и палмитоил-CoA. Тези съединения са ключови в метаболизма на въглехидратите и липидите, при преноса на ацилни групи и при синтеза и разграждането на мастни киселини. В мастно-киселинния синтез растящият веригов фрагмент е свързан с АСР (acyl carrier protein) чрез тиоестерна връзка, което позволява лесно прехвърляне и удължаване на веригата.
Тиоестери също играят роля при посттранслационни модификации на белтъци — например S-ацилтирането (палмитоилиране) на цистеинови остатъци регулира локализацията и функцията на много протеини.
Реактивност и механизми
Поради по-слабото резонансно делокализиране на серния атом, тиоестерните карбонили са по-податливи на нуклеофилно атакуване от тези при естери или амиди. Това ги прави по-добри ацил-донори в ензимни и химични реакции — разграждането (хидролиза) на тиоестер дава карбоксилна киселина и тиол, и често е енергетично по-изгодно отколкото хидролизата на обикновен естер. Вследствие на това много ензимни трансакциите използват тиоестери като «високоенергийни» междинни продукти.
Тиоестерите образуват стабилни енолати при алкилиране или при участието им в Клайзонова (Claisen) конденсация и други реакционотворни стъпки, които органичните химици използват за изграждане на сложни молекули. Освен това тиоестерите се използват при трансфера на ацилни групи и в технологии като native chemical ligation за синтез на пептиди и белтъци.
Приложения в синтеза и медицина
В органичния синтез тиоестерите служат като удобни ациловарианти — те участват в паладиеви крос-купинги, редукции до кетони (напр. реакция с органокупруматни реагенти), и в стратегии за стереоспецифична алкилиране. В пептидна химия тиоестерите на C-края на пептиди са ключови за нативна химична лигация, която позволява свързване на две пептидни вериги чрез образуване на естествена пептидна връзка.
В биомедицинския контекст манипулацията на S-ацилтирането и ацетилацията (чрез ацетил-CoA) е важна за проучване на клетъчен метаболизъм, епигенетика и патофизиология на заболявания.
Стабилност и безопасност
Тиоестерите обикновено са по-реактивни към хидролиза и нуклеофилни атаки отколкото съответните им естери, но техният реален живот и стабилност зависят от стеричните и електронните ефекти на заместителите. Някои тиоестери имат характерен мирис (тиоли са мирисни), и при работа с тях в лаборатория трябва да се спазват стандартни мерки за безопасност — добра вентилация, предпазни ръкавици и очила.
Кратко резюме: Тиоестерите са важна група съединения със структура, подобна на естерите, но със серен атом на мястото на кислорода. Това променя тяхната електроника и реактивност — прави ги по-добри ацилни донори и ключови междинни продукти в биохимията и в органичния синтез.