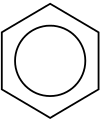
Ароматният въглеводород, или арен, е съединение с въглеводороден пръстен. В него се редуват двойни и единични връзки между въглеродните атоми, които образуват пръстени. Много от съединенията имат сладък аромат, откъдето идва и терминът "ароматни". Пръстенът от шест въглеродни атома в ароматните съединения е известен като бензенов пръстен, по името на най-простия възможен въглеводороден пръстен - бензена. Ароматните въглеводороди могат да бъдат моноциклични (MAH) или полициклични (PAH).
Някои съединения на небензенова основа, наречени хетероарени, които следват правилото на Хюкел, също са ароматни съединения. В тези съединения поне един въглероден атом е заменен с един от кислорода, азота или сярата.
Какво означава "ароматност" — структурна и електронна характеристика
Ароматността не се отнася само до миризма, а до специфична електронна конфигурация. Ароматните пръстени са циклични, планарни и имат конюгирана система от π-електрони, която се делокализира над целия пръстен. Това делокализиране дава допълнителна стабилност на молекулата — т.нар. ароматна стабилизация.
- Делокализация: въглеродните атоми в пръстена образуват споделена π-електронна облачност, вместо отделни двойни връзки.
- Резонанс: ароматните съединения често се представят чрез резонансни структури; реалната структура е хибрид между тях.
- Планарност: за да има ефективна π-делокализация, атомите трябва да лежат приблизително в една равнина.
Критерии за ароматичност (правило на Хюкел)
За да се определи дали едно циклично конюгирано съединение е ароматно, се използва правилото на Хюкел. Съществените условия са:
- Циклична, конюгирана система (всяка атомна единица участва с p-орбитал).
- Планарна или почти планарна геометрия.
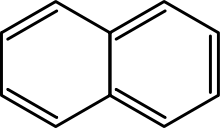
- Наличност на (4n + 2) π-електрона (където n = 0, 1, 2 ...). Примери: 6 π-електрона за бензен (n = 1), 10 π-електрона за нафтален (n = 2) и т.н.
Съществуват и противоположни понятия: антиароматични (с 4n π-електрона — нестабилни и реактивни) и неароматични (липса на конюгация или планарност).
Примери на ароматни съединения
- Бензен (C6H6) — класическият пример; равномерно разпределени π-електрони по шестчленния пръстен.
- Толуен, фенол, анилин — производни на бензена със заместители (алкилна, хидроксилна, аминогрупа).
- Нафтален (C10H8), антрацен и фенантрен — полициклични ароматни въглеводороди (PAH) с два или повече кондензирани бензенови пръстена.
- Хетероарени — пиридин, пирол, фуран, тиофен; в тези пръстени един или повече въглеродни атоми са заместени с азот, кислород или сяра, но системата остава ароматна при спазване на условието за π-електрони.
Химични реакции
Ароматните системи проявяват характерна реакционна способност:
- Електрофилно ароматично заместване (ЕАЗ): основен тип реакции за бензеновия пръстен — нитриране, сулфониране, халогениране, Friedel–Crafts алкилиране/ацилане. Пръстенът запазва ароматичността си след заместването.
- Хидрогениране: при наличие на подходящ катализатор ароматичният пръстен може да се редуцира до циклоалкани (това изисква енергия и специфични условия).
- Окисление: някои заместители на бензен (напр. алкилни групи) могат да се окислят до карбоксилни киселини; полицикличните ароматни въглеводороди могат да образуват токсични окислени продукти.
Физически свойства и аналитични признаци
- Ароматните пръстени имат характерни UV-Vis и NMR спектрални особености — например протоните на ароматния пръстен в 1H NMR се явяват в зоната на понизено поле (6–8 ppm) поради магнитното поле на π-електроните.
- Като правило, ароматните въглеводороди са по-стабилни и със сравнително високи точки на кипене/топене в сравнение с изоенични ациклични аналогични съединения.
Приложения
Ароматните съединения играят голяма роля в химичната промишленост и всекидневието:
- Изходни суровини за синтез на бои, препарати, фармацевтични продукти и пластмаси.
- Разтворители (напр. бензен — макар че използването му е ограничено заради токсичност).
- Компоненти на горива и лубриканти; PAH се срещат в продуктите от непълно изгаряне.
Опасности и екологични аспекти
- Токсичност: някои ароматни въглеводороди са високо токсични или канцерогенни (напр. бензен е известен като причинител на левкемия; много PAH като бензо[a]пирен са канцерогенни).
- Загрязняване: PAH се акумулират в почви и седименти и са продукт от непълно изгаряне (тютюн, автомобилни емисии, горене на дърва и въглища).
- Поради това има строги регулации за емисии и използване на някои ароматни съединения.
Как се определя ароматичността в практиката
- Спектроскопски методи: NMR (характерни химични измествания), UV-Vis (конюгирани системи), IR.
- Структурно: рентгенова кристалография за измерване на дължините на връзките — при ароматни пръстени дължините са усреднени между единична и двойна връзка.
- Теоретични и калкулационни методи: изчисляване на ароматичната енергия и електронна структура с помощта на квантово-химични методи.
Кратко обобщение: ароматните въглеводороди (арени) са циклични, конюгирани и планарни системи с делокализирани π-електрони, които следват правилото на Хюкел (4n + 2 π-електрона). Те имат специфични физико-химични свойства, широка употреба, но и потенциални рискове за здравето и околната среда.