pH (рН) — какво е, формула и стойности на скалата
Научете всичко за pH: какво е, формула, скала 0–14, стойности и интерпретация. Прости обяснения, примери и как да измерите киселинност/алкалност.
pH е скала за киселинност, която обикновено се описва от 0 до 14. Тя показва колко киселинно или алкално е дадено вещество или разтвор. По-киселите разтвори имат по-ниско pH, по-алкалните — по-високо. Веществата, които не са нито кисели, нито алкални (т.е. неутрални разтвори), обикновено имат pH около 7. Киселините имат pH по-малко от 7, а алкалите — pH по-голямо от 7.
Какво точно измерва pH? pH е мярка за концентрацията на протони (H+) в разтвора. Понятието е въведено от С. П. Л. Сьоренсен през 1909 г. Буквата "p" произлиза от немската дума potenz (в превод — степен или показател), а "H" означава водороден йон (H+), т.е. измерва се „степента“ на водородните йони в разтвора.
Най-разпространената формула за изчисляване на pH е:
pH = - log 10 [ H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}
В израза [H+] означава концентрацията на H+ йони (често се пише и като [H3O+], равна на концентрацията на хидрониевите йони), измерена в молове на литър (моларитет). Тъй като логаритъмът е с основа 10, промяна от единица в pH отговаря приблизително на десеткратно изменение в концентрацията на H+.
Правилното уравнение обаче всъщност е:
pH = - log 10 [ a H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}
където a H + {\displaystyle a_{\mathrm {H^{+}} }}
Примери за стойности на pH
- Силно киселинни разтвори: pH приблизително 0–2 (например 1 M HCl има pH ≈ 0).
- Слабо киселинни течности: pH ≈ 3–6 (например оцет — около pH 2.5–3).
- Неутрални: pH ≈ 7 (дистилирана вода при 25 °C има pH ≈ 7).
- Слабо алкални: pH ≈ 8–11 (например морската вода около pH 8).
- Силно алкални: pH ≈ 12–14 (например концентрирани разтвори NaOH).
Повечето вещества имат pH в диапазона от 0 до 14, въпреки че изключително киселинни или алкални вещества могат да имат pH < 0 или pH > 14 (това се получава при много високи концентрации на силни киселини или основания).
Измерване на pH
- Електронни pH-метри: измерват електроден потенциал и дават точна стойност; изискват калибрация и поддръжка на електрода.
- Индикатори и индикаторни хартии: цветни реактиви или хартиени ленти, удобни за бърза и приблизителна оценка (например лакмус).
- Химични индикатори: вещества, които променят цвета си при определени pH диапазони (напр. фенолфталеин).
Значение на pH
pH е важен в много области:
- В биологията: клетъчните процеси и ензимната активност са чувствителни към pH; кръвта на човека се поддържа около pH 7.35–7.45.
- В екологията: pH на почвите и водите влияе на живота на растенията и водните организми (например риба не понася силно кисели езера).
- В индустрията и дома: прането, почистването, хранителната обработка, фармацията и много технологични процеси изискват контрол на pH.
- В химията: реакциите на кислород/водород, корозията, разтворимостта на вещества и равновесието ионни равновесия зависят от pH.
Други важни бележки
- Логаритмична природа: промяна с 1 единица pH означава 10 пъти по-голяма или по-малка концентрация на H+.
- Температурна зависимост: стойността на pH и константата на йонизация на водата се променят с температурата; затова при прецизни измервания трябва да се посочва температурата.
- Буферни разтвори: смеси, които противодействат на големи промени в pH при прибавяне на киселина или основа; важни за биологичните системи и лабораторните условия.
- Алкални йони: алкалните разтвори имат вместо водородни йони по-висока концентрация на хидроксидни йони (OH-); връзката между [H+] и [OH-] в чиста вода при 25 °C е [H+][OH-] = 10^(-14).
Тази информация дава общ и практичен преглед на понятието pH, неговата физическа значимост, начини за измерване и приложения. За по-напреднали изчисления и лабораторни условия е важно да се има предвид активността на йоните, температурата и йонната сила на разтвора.
Индикатори за рН
Някои багрила променят цвета си в зависимост от това дали се намират в киселинен или в алкален разтвор. pH индикаторът е химично съединение, което се добавя в малки количества към разтвор, за да може да се види pH (киселинността или основността) на разтвора. Индикаторът за рН е химически детектор за хидрониеви йони (H3O+) или водородни йони (H+). Обикновено индикаторът променя цвета на разтвора в зависимост от рН.
Типични индикатори са фенолфталеин, метилово оранжево, метилово червено, бромотимолово синьо и тимолово синьо. Всеки от тях променя цвета си в различни точки на pH скалата и може да се използва заедно като универсален индикатор.
Друг начин е да се използва лакмусова хартия, която се основава на естествен индикатор за рН. Хартията може да ви покаже колко силен е химикалът, дали е по-силна киселина или по-силна основа.
Някои често срещани стойности на pH
| pH | |
| Батерийна киселина | 0 |
| Стомашна киселина | 1.0 |
| Лимонов сок | 2.4 |
| Кола | 2.5 |
| Кислородна вода | 2.5 - 3.0 |
| Оцет | 3.0 |
| Портокалов или ябълков сок | 3.0 |
| Бира | 4.5 |
| Кафе | 5.0 |
| Мляко | 6.6 |
| 7.0 | |
| Кръв | 7.35 - 7.45 |
| Обикновен шампоан | 8.0 |
| Морска вода | 8.0 |
| Постоянна вълна | 8.5 - 9.2 |
| Сапун за ръце | 9.0 - 10.0 |
| Боя за коса | 9.5 - 10.5 |
| Магия направо | 11.5 |
| Домакински амоняк | 11.5 |
| Избелване | 12.3 |
| Сода каустик | 12.7 |
| Домашна луга | 13.5 |
| Препарат за почистване на канали | 14 |
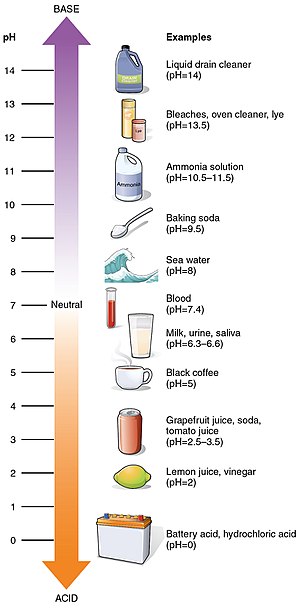
Стойности на pH на някои често срещани вещества
Неутрализация
Неутрализацията може да се обобщи с уравнението:
H+
+ OH-
→ H
2O
Свързани страници
Въпроси и отговори
В: Какво е рН?
О: pH е скала за киселинност от 0 до 14, която измерва концентрацията на протони (H+) в разтвор. Тя показва колко киселинно или алкално е дадено вещество, като по-киселите разтвори имат по-ниско pH, а по-алкалните - по-високо pH. Неутралните разтвори обикновено имат рН 7.
Въпрос: Кой въвежда понятието pH?
О: С.П.Л. Сьоренсен въвежда това понятие през 1909 г.
В: Какво означава буквата "р" в "pH"?
О: "p" означава немската дума potenz, което означава сила или концентрация.
В: Как се изчислява рН?
О: Най-разпространената формула за изчисляване на рН е да се вземе отрицателният логаритъм на 10-кратната концентрация на H+ йони (изписвани също [H3O+], което показва равни концентрации на хидрониеви йони), измерена в молове на литър (или моларитет). Съществува обаче и уравнение, което взема предвид активността, а не само концентрацията, което може да даде различни стойности от по-често използваната формула в зависимост от ситуацията.
Въпрос: Какъв е диапазонът на повечето вещества в скалата за рН?
О: Повечето вещества имат рН между 0 и 14, въпреки че изключително кисели или алкални вещества могат да имат стойност извън този диапазон (по-малка от 0 или по-голяма от 14).
В: По какво се различават алкалните вещества от киселинните в скалата за рН? О: Алкалните вещества имат по-високи стойности по скалата поради концентрацията на хидроксидни йони (OH-) вместо на водородни йони, както е при киселините.
обискирам
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)