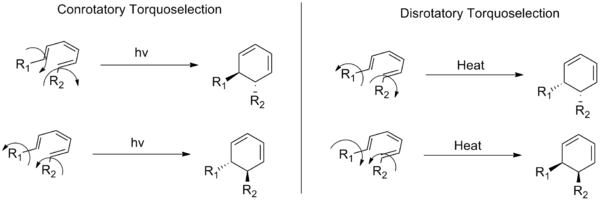
Конротационен и дистротационен описват два начина, по които се извършват електроцикличните реакции — вид електроциклични реакции в рамките на органичната органични химични реакции). При конротационния режим заместителите, разположени в краищата на конюгирана система от двойни връзки, се въртят в една и съща посока (или и двете по часовниковата стрелка, или и двете обратно на нея) по време на отварянето или затварянето на пръстена. При дистротационния режим крайните орбитали се въртят в противоположни посоки.
Какво определя режима — орбитална симетрия
Ключът е в симетрията на най-високо заетата молекулна орбитала (HOMO) на линейната (отворена) конюгирана система. За да се образува нова σ-връзка при затварянето на пръстен, фазите (знаците) на крайните пи-орбитали трябва да се подредят по определен начин. Ако фазите в HOMO изискват крайните орбитали да се въртят в противоположни посоки, реакцията е дистротационна; ако изискват едновременно въртене в една и съща посока, реакцията е конротационна.
Правила за броя на π-електроните и типа на стимула
- Термични (термални) електроциклични реакции:
- Ако системата има 4n + 2 π-електрона (Hückel-стабилна, напр. 6 π e−), то затварянето/отворянето е стереоспецифично и обикновено следва дистротационен режим.
- Ако системата има 4n π-електрона (напр. 4 или 8 π e−), реакцията обикновено е конротационна.
- Фотоиндуцирани (светлинно активирани) електроциклични реакции:
- Правилата се обръщат — 4n + 2 системи предпочитат конротация, а 4n системи — дистротация.
Пример
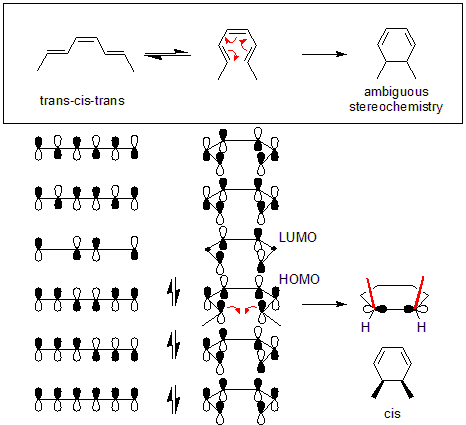
Класически пример е превръщането на транс-цис-транс-2,4,6-октатриен в цис-диметилциклохексадиен. Този октатриен има 6 π-електрона (4n + 2, с n = 1), затова орбиталната механика на термичната реакция изисква дистротационен режим — крайните пи-орбитали се въртят в противоположни посоки, за да се получи правилната симетрия на образуващата се σ-връзка в цикличния продукт. По този начин се запазва орбиталната симетрия, което обяснява и стереоспецифичността на процеса.
Практически последици и обобщение
Поради запазването на орбиталната симетрия, електроцикличните реакции са стереоспецифични — ориентацията на заместителите в продукта е предопределена от режима (конротация или дистротация). Тези правила се формулират и обобщават от Правилата на Удуърд–Хофман, които позволяват да се предскаже стереохимията на електроцикличните трансформации въз основа на броя на π-електроните и дали процесът е термичен или фотохимичен.
По-долу илюстрацията показва разликата между конротационните и дистротационните механизми и как въртенето на краищата на конюгираната система влияе върху крайната стереохимия на продукта.