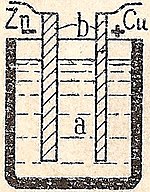
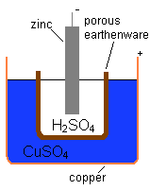
Химическата клетка преобразува химическата енергия в електрическа. Повечето батерии са химически клетки. В батерията протича химическа реакция, която предизвиква протичане на електрически ток. В основата стоят два електрода (анод и катод) и електролит — веществото, което позволява преноса на йони вътре в клетката, докато електроните преминават през външната верига и захранват потребителите.
Видове батерии
Съществуват два основни вида батерии - акумулаторни и неакумулаторни (первични).
- Неакумулаторни (первични) батерии — не могат да се презареждат. Те доставят енергия, докато активните химикали се изразходват, след което се изхвърлят. Чести типове: цинк-въглеродни, алкални, някои литиеви одноразови клетки. Подходящи за устройства с нисък ток на разряд или когато презареждането не е практично.
- Акумулаторни (вторични) батерии — могат да се зареждат повторно чрез обратен ток, който възстановява първоначалните химични състави. Типични примери: оловно-киселинни (lead-acid), никел-кадмиеви (NiCd), никел-металхидридни (NiMH), литиево-йонни (Li-ion). Тези батерии са предпочитани за автомобилни акумулатори, преносими устройства, електромобили и стационарни системи за съхранение на енергия.
Кратка история
Първите практични акумулатори са разработени в средата на XIX век. Французинът Гастон Планте (Gaston Planté) е известен с изобретяването и усъвършенстването на оловно-киселинния акумулатор през 1859 г., който остава в основата на автомобилните батерии до днес.
Принцип на работа
Батерията работи чрез окислително-редукционни (редокс) реакции между електродите и електролита. При разреждане:
- На анода протича окисление — електрони се освобождават и текат през външната верига към натоварването.
- На катода протича редукция — електроните се приемат след преминаване през външната верига.
- Вътрешно, йони в електролита компенсират заряда, като мигрират между електродите.
При акумулаторните клетки, при подаване на външен ток в обратна посока, химическите реакции могат да се обърнат и батерията да бъде възстановена (заредена).
Основни характеристики
- Номинално напрежение на клетка: например 1,5 V (алкални), 1,2 V (NiCd/NiMH), 2,0 V (оловно-киселинни), 3,6–3,7 V (Li-ion).
- Капацитет: измерва се в ампер-часове (Ah) или милиампер-часове (mAh) и показва колко заряд може да достави батерията при определени условия.
- Енергийна плътност: количество енергия на единица маса или обем — важна за преносими устройства и електромобили.
- Вътрешно съпротивление: влияе на способността за подаване на високи токове и загубите при протичане на ток.
- Саморазряд: постепенна загуба на заряд при съхранение — различава се в зависимост от химията (алкални по-нисък саморазряд, NiCd високо, Li-ion ниско).
- Живот в цикли: броят на пълни зареждания/разреждания, които батерията може да понесе преди значително снижаване на капацитета.
Приложения
- Малки джаджи: часовници, дистанционни, фотоапарати.
- Преносима електроника: телефони, лаптопи (често Li-ion).
- Автомобили: стартови оловно-киселинни батерии; електромобили използват големи Li-ion пакети.
- Индустриални и военни приложения: резервно захранване, подводници — Подводниците често имат много големи акумулатори за подводно плаване.
- Съхранение на енергия в мрежата: големи стелажи батерии за балансиране на възобновяеми източници.
Съединяване на клетки
За постигане на по-високо напрежение или капацитет, клетки се свързват:
- Последователно (series) — напреженията се сумират.
- Паралелно (parallel) — капацитетът (Ah) се увеличава, а напрежението остава същото.
Грижа, безопасност и зареждане
- Използвайте правилен заряден режим и зарядни устройства, предназначени за конкретната химия (напр. Li-ion зареждащи устройства поддържат специфични напрежения и защити).
- Избягвайте презареждане и пълно разреждане — те съкращават живота на акумулатора. Някои технологии (например NiCd) са чувствителни към "memory effect", при който капацитетът намалява при повтарящи се частични зареждания; NiMH и Li-ion имат по-малък или нулев този ефект.
- Дръжте батериите далеч от високи температури и огън — при някои типове (особено повредени Li-ion) е възможно термично бягство (thermal runaway) и пожар.
- Не късайте полюсите и не използвайте повредени батерии.
- При оловно-киселинни акумулатори с течен електролит проверявайте нивото и използвайте защитни средства при обслужване.
Околна среда и рециклиране
Много батерии съдържат материали, които са вредни за околната среда (олово, кадмий, литий и др.). Затова е важно правилното им изхвърляне и рециклиране. Оловно-киселинните батерии, например, имат добре развита система за рециклиране, докато за литиево-йонните се работи усилено да се подобри рециклирането и възстановяването на материали.
Заключение
Батериите са ключов компонент на модерната техника — от малки еднократни клетки до големи акумулаторни системи за автомобили и подводници. Правилният избор на тип батерия, правилната експлоатация и рециклиране са важни за дълъг живот, безопасност и опазване на околната среда.