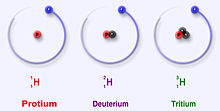
Водородът има три основни изотопа: протий (1H), деутерий (2H) и тритий (3H). Тези изотопи се образуват естествено в природата. Протият и деутерият са стабилни. Тритият е радиоактивен и има период на полуразпад от около 12 години. Учените са създали четири други изотопа на водорода (4H to 7H), но тези изотопи са много нестабилни и не съществуват в природата.
Основните изотопи на водорода са уникални, тъй като са единствените изотопи, които имат име. Тези имена се използват и днес. Понякога деутерият и тритият получават свои собствени символи - D и T. Международният съюз по чиста и приложна химия обаче не харесва много тези имена, въпреки че те често се използват. Има и други изотопи, които са имали свои собствени имена, когато учените са изучавали радиоактивността. Но днес техните имена вече не се използват.
Атомна структура и маси
Разликата между изотопите е броят на неутроните в ядрото. Протият (1H) има само един протон и няма неутрони. Деутерият (2H) има един протон и един неутрон. Тритият (3H) има един протон и два неутрона. Това води до различни маси и физични свойства: масите (атомни масови единици) са приблизително 1.0078 u за 1H, 2.0141 u за 2H и 3.0160 u за 3H.
Естествено разпределение и произход
В природата най-разпространеният изотоп е протият — около 99.98% от водородните атоми. Деутерият е рядък, но стабилен — негова естествена изобилие е приблизително 0.015–0.016% (около 150–160 части на милион). Тритият се среща в много малки количества, образува се в горните слоеве на атмосферата при взаимодействие на космическите лъчи с азота и кислорода, и също се произвежда в ядрени реактори и водород-ядрени експерименти.
От гледна точка на космологията, количеството деутерий, създадено по време на големия взрив (Big Bang nucleosynthesis), е важен показател за плътността на барионите във Вселената — наблюденията на деутерий помагат да се проверят модели за ранната космология.
Физични и химични различия
Въпреки че химическият атом на водорода участва в същите връзки, масовите разлики между изотопите причиняват значими ефекти:
- Кинетичен изотопен ефект — химичните реакции с участието на деутерий протичат по-бавно заради по-силните и по-малко податливи на разкъсване връзки D–X спрямо H–X.
- Физични параметри — например, тежката вода (D2O) има малко по-високи точки на топене (≈3.82 °C) и кипене (≈101.4 °C) и по-висока плътност от обикновената вода (H2O).
- Спектроскопия — честотите на вибрационните и ротационните преходи се преместват, което се използва в аналитични методи и в материя-спектра за проследяване на изотопни замествания.
Приложения
Изотопите на водорода имат множество практични приложения:
- Деутерий — използва се за производство на тежка вода (D2O), която служи като модератор в някои типове ядрени реактори (например CANDU). Деутерият се използва и като маркер в химични и биологични изследвания (деутерирани съединения), в НМК (деутерирани разтворители като D2O или CDCl3 за входна честота/lock) и за стабилно изследване на механизми на реакции.
- Тритий — радиоактивен бета-емитер, използван при осветителни елементи (самосветещи знакчета), при производство на термонуклеарно гориво (D–T синтеза в изследванията за контролирана термоядрена енергия), и в радиолаборатории като източник за маркиране и следене. Тритият се произвежда промишлено в ядрени реактори и чрез реакции с литиум.
- Научни изследвания — и двата изотопа се използват в изследвания на механизми на химични реакции, в проследяване на метаболитни пътища и във физиката на плазмата и термоядрените реакции (D–T реакцията освобождава около 17.6 MeV енергия: D + T → 4He + n + 17.6 MeV).
Риск и безопасност
Тритият е бета-излъчител с ниска енергия; неговата радиация не прониква през кожата, но е опасен ако се погълне, вдиша или влезе в биологични молекули (тъй като лесно се свързва с водата и органичните вещества). Работата с тритий изисква специални предпазни мерки и контрол на изпускането, за да се предотврати замърсяване на околната среда и попадане в човешкия организъм.
Редки нестабилни изотопи (sup>4H до sup>7H)
Учени са синтезирали много краткотрайни, екстремно нестабилни изотопи на водорода като 4H, 5H, 6H и 7H в експериментални условия. Тези ядра са силно неутронно-наситени и обикновено са неустойчиви спрямо отделяне на неутрони или друг разпад — те живеят изключително кратко (често в порядъка на микросекунди до фемтосекунди в зависимост от изотопа и начина на наблюдение) и не се срещат в природата. Изследването им помага да се опознаят ядрени сили и границите на стабилността на ядрата.
Обобщение
Протият, деутерият и тритият са трите главни изотопа на водорода с важни физични, химични и приложни особености. Протият е най-разпространен и най-лек, деутерият — стабилен и полезен за промишлени и научни приложения, а тритият — радиоактивен и важен в ядрените технологии и изследванията по термоядрен синтез. По-екзотичните изотопи от 4H нагоре са предмет на фундаментални изследвания по ядрена физика.